
分析 (1)Cl2和H2O反应生成氯化氢和次氯酸;
(2)氯气具有强的氧化性,能够氧化亚硫酸根离子生成硫酸根离子;
(3)乙醇与乙酸在浓硫酸作用下反应生成乙酸乙酯;
(4)Cu2Y为氧化亚铜,+1价的铜具有还原性,硝酸具有氧化性,二者发生氧化还原反应生成硝酸铜和二氧化氮和水.
解答 解:(1)Cl2和H2O反应生成氯化氢和次氯酸,化学方程式:Cl2+H2O=HCl+HClO;
故答案为:Cl2+H2O=HCl+HClO;
(2)氯气与亚硫酸钠溶液反应生成硫酸钠和氯化氢,离子方程式:Cl2+SO32-+H2O═SO42-+2H++2Cl-;
故答案为:Cl2+SO32-+H2O═SO42-+2H++2Cl-;
(3)乙醇与乙酸在浓硫酸作用下反应生成乙酸乙酯,方程式:CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
故答案为:CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(4)Cu2Y为氧化亚铜,Cu2O与浓硝酸反应生成红棕色的气体NO2,该反应的方程式为:Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O,
故答案为:Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O.
点评 本题考查了化学方程式、离子方程式的书写,明确物质的性质及发生反应的实质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | SO2、SO3都是极性分子 | |
| B. | 在H3O+和[Cu(H2O)4]2+中都存在配位键 | |
| C. | 元素电负性越大的原子,该元素的原子吸引键合电子的能力越强 | |
| D. | 原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{19}^{40}$K与${\;}_{20}^{40}$Ca | B. | 正丁烷与异丁烷 | ||
| C. | ${\;}_{19}^{40}$K与${\;}_{19}^{39}$K | D. | 金刚石与石墨 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,4.6 g NO2气体约含有1.81×1023个原子 | |
| B. | 在标准状况下,80 gSO3所占的体积约为22.4L | |
| C. | 常温下,0.1 mol/L醋酸溶液的pH约为1 | |
| D. | 标准状况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O原子的电子排布图为 | |
| B. | 氯化钠的分子式:NaCl | |
| C. | Cl-的结构示意图: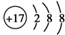 | |
| D. | Ca原子的电子排布式为 1s22s22p63s23p63d2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用倾析法分离时,将烧杯中的上层清液用玻璃棒引流到另一容器内,即可使沉淀与清液分离 | |
| B. | 洗涤沉淀时,应在过滤器中加入洗涤液浸没沉淀,过滤,并重复2到3次 | |
| C. | 抽滤完毕,应先拆下连接抽气泵和吸滤瓶的橡胶管,再关闭水龙头,最后将滤液从吸滤瓶支管口倒出 | |
| D. | 用移液管取液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,B
,B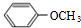 ,C
,C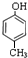 .
. ,②
,②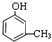 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com