
| 酸\反应进程\ | 1min | 2 min | 3 min | 4 min | 5 min |
| 3.0mol/L HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 1.5 mol/L H2SO4 | 产生的气泡很少 | ||||
| 3.0mol/L H2SO4 | 产生的气泡很少 | ||||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe与稀H2SO4反应放出气体:Fe+6H+=2Fe3++3H2↑ |
| B、稀H2SO4与BaCl2溶液反应生成沉淀:Ba2++SO42-═BaSO4↓ |
| C、用大理石与稀盐酸制备CO2:CaCO3+2H+=Ca2++CO2↑+H2O |
| D、碳酸钠溶液与足量稀盐酸:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤⑥ | B、②④⑥ |
| C、①③⑤ | D、①②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③⑤ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入氯化钡溶液,有白色沉淀生成,再加稀硝酸,沉淀不溶解 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入硝酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| C | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该溶液一定含有CO32- |
| D | 向某溶液中加入NaOH溶液并微热,产生能够使湿润的红色石蕊试纸变蓝的无色气体 | 该溶液中一定含有NH4+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
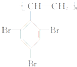 )是性能优良的阻燃剂,其两种合成工艺如图所示.
)是性能优良的阻燃剂,其两种合成工艺如图所示.
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 催化剂(1g) | … | |||
| 1 | α-Fe2O3 | ||||
| 2 | γ-Fe2O3 | ||||
| 3 | MnO2 | ||||
| ﹕ ﹕ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的密度不再发生变化 |
| B、反应过程中v(N2):v(H2)=1:3 |
| C、反应过程中c(N2):c(H2):c(NH3)=1:3:2 |
| D、单位时间内断开a mol H-H键的同时断开2a mol N-H键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com