
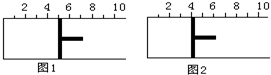
 如图所示,一定条件下将lmolA气体和3molB气体充入一个体积可变的密闭容器中,可滑动活塞的位置图1所示.在恒温恒压下发生A(g)+3B(g)?2C(g),当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率为( )
如图所示,一定条件下将lmolA气体和3molB气体充入一个体积可变的密闭容器中,可滑动活塞的位置图1所示.在恒温恒压下发生A(g)+3B(g)?2C(g),当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率为( )| A. | 20% | B. | 40% | C. | 50% | D. | 无法确定 |
分析 恒温恒压下气体的体积与物质的量成正比,设平衡时物质的量为n,则$\frac{1mol+3mol}{5V}$=$\frac{n}{4V}$,解得n=3.2mol,该反应物质的量减少4mol-3.2mol=0.8mol,结合差量法计算.
解答 解:恒温恒压下气体的体积与物质的量成正比,设平衡时物质的量为n,则$\frac{1mol+3mol}{5V}$=$\frac{n}{4V}$,解得n=3.2mol,该反应物质的量减少4mol-3.2mol=0.8mol,设转化的A为x,
A(g)+3B(g)?2C(g)△n
1 2
x 0.8mol
$\frac{1}{x}=\frac{2}{0.8mol}$,
解得x=0.4mol,
则平衡时A的转化率为$\frac{0.4mol}{1mol}$×100%=40%,
故选B.
点评 本题考查化学平衡的计算,为高频考点,把握平衡时物质的量、差量法计算为解答的关键,侧重分析与计算能力的考查,注意阿伏伽德罗定律的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
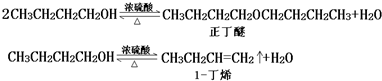
| 化合物 | 密度(g•cm-3) | 水溶性 | 沸点(℃) |
| 冰乙酸 | 1.05 | 易溶 | 118.1 |
| 正丁醇 | 0.80 | 微溶 | 117.2 |
| 正丁醚 | 0.77 | 不溶 | 142.0 |
| 乙酸正丁酯 | 0.90 | 微溶 | 126.5 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
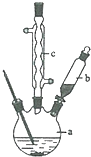 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: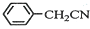 +H2O+H2SO4$\stackrel{100~130℃}{→}$
+H2O+H2SO4$\stackrel{100~130℃}{→}$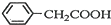 +NH4HSO4
+NH4HSO4 +Cu(OH)2→(
+Cu(OH)2→(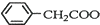 )2Cu+H2O
)2Cu+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CxHy(l)+(x+$\frac{y}{4}$)O2(g)=xCO2(g)+$\frac{y}{2}$H2O(l)△H=($\frac{10Q}{9}$-1366.8)kJ•mol-1 | |
| B. | CxHy(l)+(x+$\frac{y}{4}$)O2(g)=xCO2(g)+$\frac{y}{2}$H2O(l)△H=(-$\frac{10Q}{9}$+1366.8)kJ•mol-1 | |
| C. | CxHy(l)+(x+$\frac{y}{4}$)O2(g)=xCO2(g)+$\frac{y}{2}$H2O(l)△H=($\frac{10Q}{9}$-151.9)kJ•mol-1 | |
| D. | CxHy(l)+(x+$\frac{y}{4}$)O2(g)=xCO2(g)+$\frac{y}{2}$H2O(l)△H=(-$\frac{10Q}{9}$+151.9)kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
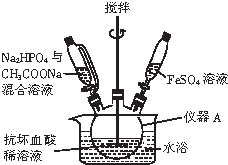 磷酸亚铁晶体[Fe3(PO4)2•8H2O]是蓝白色单斜晶体,溶于稀强酸,不溶于水、醋酸、醇,主要用于制作磷酸铁锉电池.实验室制备磷酸亚铁晶体的装置、反应原理和实验步骤如下:
磷酸亚铁晶体[Fe3(PO4)2•8H2O]是蓝白色单斜晶体,溶于稀强酸,不溶于水、醋酸、醇,主要用于制作磷酸铁锉电池.实验室制备磷酸亚铁晶体的装置、反应原理和实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )| A. | 只有① | B. | 只有②④ | C. | 只有①②④ | D. | 只有①和③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铷比镁金属性强 | |
| B. | 氯化镁比氯化铷难溶 | |
| C. | 高温下,镁离子得电子能力比铷离子弱 | |
| D. | 铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-H | C═C | C-C | H-H |
| 键能/kJ•mol-1 | 414.4 | 615.3 | 347.3 | 435.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | 温度℃ | 压强/kPa | CH4初始浓度/mol•L-1 | H2O初始浓度/mol•L-1 |
| 1 | 400 | p | 3.0 | 7.0 |
| 2 | t | 101 | 3.0 | 7.0 |
| 3 | 400 | 101 | 3.0 | 7.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com