
Fe、Cu都是人类最早使用的金属。某校化学研究性学习小组的同学运用实验手段研究Fe、Cu的相关性质,请你参与研究并完成下列各题:
(1)甲同学取一束细铜丝用砂纸打磨后放在酒精灯上加热至红热,然后迅速伸入盛Cl2的集气瓶中。你认为甲同学在实验中应该观察到的现象是__________
_________________________________________________________________。
(2)乙同学为探究Fe在冷浓硝酸和热浓硝酸中的反应情况,设计了如图所示的实验装置:
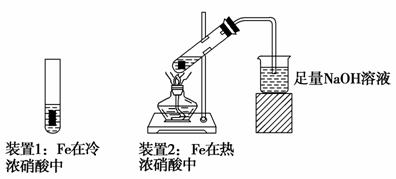
①乙同学发现装置1中Fe未溶解,其原因是_____________________________
_________________________________________________________________;
②装置2生成的气体(假定为NO2和NO混合气体)全部通入100 mL 4 mol·L-1 NaOH溶液,恰好被完全吸收,反应为:NO+NO2+2NaOH===2NaNO2+H2O 2NO2+2NaOH===NaNO2+NaNO3+H2O
若生成NaNO3和NaNO2物质的量之比为1∶3,则混合气体中NO2和NO的体积比为________。
(3)丙同学在Fe和浓硝酸反应后的溶液中加入一块Cu片,Cu片先逐渐溶解,反应一段时间后不再溶解。
①丙同学依据反应现象得出Cu片溶 解的原因是和HNO3发生反应。他依据的反应现象是_______________________________________________________
解的原因是和HNO3发生反应。他依据的反应现象是_______________________________________________________
_________________________________________________________________。
②丁同学认为丙同学的结论不完全正确,他的理由是_____________________
_________________________________________________________________。
(4)请你设计实验证明(3)反应后的溶液中只含Fe2+而不含Fe3+。说明具体实验操作和实验现象:___________________________________________________
_________________________________________________________________。
解析 (1)Cu在Cl2中燃烧的现象是生成棕色的烟。
(2)①铁、铝在常温下遇到浓硫酸、浓硝酸会发生钝 化;②从化学方程式可以看出:
化;②从化学方程式可以看出:
2NO2+2NaOH===NaNO2+NaNO3+H2O
2 1 1
NO+NO2+2NaOH===2NaNO2+H2O
1 1 2
混合气体中NO2和NO的体积比为3∶1。
(3)①若试管内出现红棕色气体或铜片表面有气泡生成就可以证明Cu片溶解的原因是和HNO3发生反应;
②Fe和硝酸反应后的溶液中有HNO3,也一定有Fe3+,而Fe3+也能和Cu反应,使Cu片溶解,所以丁同学认为丙同学的结论不完全正确。
(4)检验Fe2+、Fe3+是常考的知识点。检验时可以取少许该溶液滴加几滴KSCN溶液,不出现血红色,再滴加适量新制氯水;出现血红色,证明溶液中只含Fe2+而不含Fe3+。
答案 (1)Cu在Cl2中燃烧生成棕色的烟
(2)①Fe在冷浓硝酸中发生钝化 ②3∶1
(3)①试管内出现红棕色气体或铜片表面有气泡生成
②Fe和浓硝酸反应后的溶液中有HNO3,也一定有Fe3+,而Fe3+也能和Cu反应,使Cu片溶解
(4)取少许该溶液滴加几滴KSCN溶液,不出现血红色,再滴适量新制氯水,出现血红色(答案合理即可)


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列各组物质中化学键的类型相同的是 ( )
A、CaCl2 MgCl2 Na2O B、H2O Na2O CO2
C、CaCl2 NaOH H2SO4 D、NH4Cl H2O CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
在研究化学反应中的能量变化时,我们通常做下面的实验:
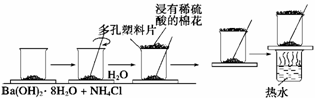
在一个小烧杯里,加入20 g已研磨成粉末的Ba(OH)2·8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10 g NH4Cl晶体,根据实验步骤,填写下表,并回答问题。
| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的___①__产生 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是_ ② 反应 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有_③___生成 |
(1)写出题目中①②③填入的内容
① ② ③
(2)实验中要立即用玻璃棒迅速搅拌的原因是: __________________。(2分)
(3)在上述实验过程中,为什么用浸有稀硫酸的湿棉花置于多孔塑料板上?(2分)
___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某地污水中含有Zn2+、Hg2+、Fe3+和Cu2+4种阳离子。甲、乙、丙3位同学设计的从该污水中回收金属铜的方案如下。
甲:

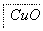
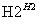
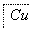
乙:
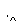


丙:



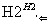
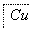
下列判断正确的是 ( )。
A.三种实验方案中都能制得纯净的铜
B.乙方案中加过量铁粉可以将4种阳离子全部还原
C.甲方案中的反应涉及置换、分解、化合、复分解4种反应类型
D.丙方案会产生环境污染
查看答案和解析>>
科目:高中化学 来源: 题型:
下面有关铜的化合物的性质叙述中正确的是( )。
A.CuSO4变成Cu SO4·5H2O是物理变化
SO4·5H2O是物理变化
B.一定条件下,新制的Cu(OH)2悬浊液能与乙醛反应但不能与乙酸反应C.CuO是黑色固体,与水反应可生成Cu(OH)2
D.Cu2O遇硝酸可能会被氧化成Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
所谓合金,就是不同种金属(也包括一些非金属)在熔融状态下形成的一种熔合物。根据下列四种金属的熔、沸点,判断其中不能形成合金的是 ( )。
| Na | Cu | Al | Fe | |
| 熔点/℃ | 97.5 | 1 083 | 660 | 1 535 |
| 沸点/℃ | 883 | 2 595 | 2 200 | 3 000 |
A.Cu和Al B.Fe和Cu
 C.Fe和Na D.Al和Na
C.Fe和Na D.Al和Na
查看答案和解析>>
科目:高中化学 来源: 题型:
有一粗硅,含杂质铁,取等质量的样品分别投入足量的稀盐酸和足量的稀氢氧化钠溶液中,放出等量的H2,则该粗硅中铁和硅的关系正确的是(提示:Si+2NaOH+H2O===Na2SiO3+2H2↑) ( )。
A.物质的量之比为:1∶1 B.物质的量之比为1∶2
C.质量之比为4∶1 D.质量之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质。已知:甲+乙===丁+己,甲+丙===戊+己;0.1 mol·L-1丁溶液的pH为13(25 ℃)。下列说法中正确的是( )。
A.原子半径:W>Z>Y>X
B.Y元素在周期表中的位置为第三周期第ⅣA族
C.1 mol甲与足量的乙完全反应共转移了1 mol电子
D.1.0 L 0.1 mol·L-1戊溶液中阴离子总的物质的量小于0.1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com