
【题目】某学生通过如图所示实验装置进行电化学实验。实验操作如下:①闭合S1,打开S2,持续20s。②打开S1,闭合S2,观察现象。下列说法不正确的是
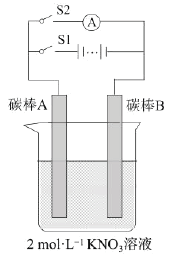
A.操作①时电极A为阳极,发生氧化反应
B.操作②时电极B为负极,电子由B处迁出
C.操作①时为电解池,操作②时为原电池
D.实验结束后,硝酸钾溶液的浓度保持不变
 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:
【题目】下列实验装置及操作均正确的是
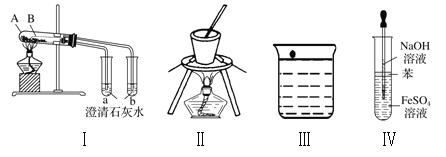
A. 图I中A盛放碳酸氢钠,B盛放碳酸钠,可对比二者的热稳定性
B. 图II可用于在碳酸钠溶液中提取碳酸钠固体
C. 图III为钠与水的反应现象探究实验的装置
D. 图IV为实验室制备观察氢氧化亚铁的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:

请回答下列问题:
(1)向操作①的滤液中滴加KSCN溶液后变为红色,则该滤液中含有______(填离子符号)。
(2)操作②中反应的离子方程式:__________________________________。
(3)操作③中反应的离子方程式:__________________________________。
(4)操作④中一系列处理的操作步骤:过滤、______、灼烧、_______、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为______g。(用含a的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学概念在逻辑上存在如图关系,对下列概念的说法正确的是( )

A. 化合物与氧化物属于交叉关系
B. 单质与非电解质属于包含关系
C. 溶液与分散系属于并列关系
D. 化合物与电解质属于包含关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠与二氧化氮能发生反应,某兴趣小组对此进行探究,提出了两种假设。
假设一:Na2O2+2NO2===2NaNO2+O2↑
假设二:Na2O2+2NO2===2NaNO3
[查阅资料]
2NaNO2+2HCl===2NaCl+NO↑+NO2↑+H2O
2NO2+2NaOH===NaNO2+NaNO3+H2O
[实验探究]
Ⅰ.按图示装置进行实验。

Ⅱ.通入二氧化氮至过氧化钠反应完全,然后对玻璃管中的固体物质进行检验。
[实验结论] 实验表明,过氧化钠与二氧化氮按“假设二”反应。
(1)过氧化钠与二氧化氮的反应中,氧化剂是____。
(2)装置A中反应的离子方程式是________。
(3)装置C的作用是__________。
(4)请设计实验证明装置B中的反应不符合“假设一”。
①实验操作:取玻璃管中的固体置于试管中,________;
②实验现象是________。
(5)有同学认为:只要直接观察C中导管口是否有气泡冒出,就可以判断B中的反应符合哪一种假设,这种想法________(填“对”或“不对”),原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习了元素周期律后,同学们对第四周期过渡元素氧化物产生了浓厚的兴趣。是否只有二氧化锰能催化氯酸钾受热分解?氧化铁、氧化铜、氧化铬等对氯酸钾的受热分解有没有催化作用?对此他们进行了实验探究。请你根据要求完成下列部分实验报告。
(1)实验仪器及试剂:实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、___、___、___等;
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾;
(2)实验步骤:略;
(3)实验数据:
实验编号 | KClO3质量(g) | 氧化物化学式 | 氧化物质量(g) | 氧化物回收率 | 产生气体(mL)(已折算到标况) | 耗时(s) |
1 | 0.60 | 10 | 480 | |||
2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
5 | 0.60 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
(4)实验讨论:
a.在氧化物的回收过程中,要进行过滤操作,所用的玻璃仪器是玻璃棒、____;
b.实验编号3的实验中KClO3的分解率为____%(保留一位小数);
c.在用Cr2O3做研究实验时,发现有黄绿色刺激性气味的气体产生,同时绿色的混合物变成了橘黄色,该刺激性气体是___(填分子式),可用____试纸检验,上述异常现象产生的原因是____;
(5)实验结论:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面物质间转换的框图,回答有关问题:

(1)写出框图中物质A、B、E、F分别指代物质的化学式:A._____________ B._____________ E._____________ F.______________
(2)如果2mol Na2O2与足量水蒸气反应,可得标准状况下气体的体积_________L;同时反应中转移电子总数是____________。(NA表示阿伏加德罗常数)
(3)如果A、B混合气体3.0g(平均摩尔质量15g·mol-1),在与G充分反应后,通过足量Na2O2层,可使Na2O2增重__________g,并得到O2_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知两种常见金属A(地壳中含量第二的金属)、B(红色金属)分别与两种酸X、Y发生反应,其转化关系如图所示,其中D为红棕色气体。
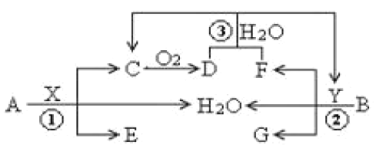
回答以下问题:
(1)反应③的离子反应方程式为___;
(2)6.4gB与过量X溶液(8mol /L、60mL)充分反应后,生成的还原产物有C、D,反应后溶液中所含X为n mol ,此时溶液中所含X的阴离子的物质的量为___mol。
(3)常温下A与Y的稀溶液能发生反应生成盐W,关于固体W的转化关系如图所示(无关物质已略去)。其中N是红棕色的化合物。

①M由两种化合物组成,其中含有F;将M通入BaCl2溶液,实验现象是___。
②若经反应I得到16 g固体N,产生的气体M恰好被0.3L1mol·L-1 NaOH溶液完全吸收得溶液1,则反应Ⅳ中发生反应的离子方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Be(OH)2是两性的,跟强酸反应时生成Be2+,跟强碱反应时生成BeO22—。现有三份等物质的量浓度、等体积的BeCl2、MgCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mol)的关系如图所示,则与BeCl2、MgCl2、AlCl3三种溶液对应的图像正确的是( )
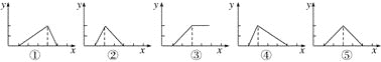
A. ⑤③① B. ②③④ C. ③⑤④ D. ③②①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com