
| A、溶液的pH=2 |
| B、c(Na+)=0.01 mol/L≥c(B2-) |
| C、c (H+)?c(OH-)=10-14 |
| D、c(Na+)+c(H+)=c(HB-)+c(B2-)+c(OH-) |


科目:高中化学 来源: 题型:
| A、构成分子晶体的微粒之间可能含有离子键 |
| B、原子晶体一定是单质 |
| C、离子晶体熔化时,需要克服离子键 |
| D、碘晶体升华时,分子中共价键发生断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将SO2、SO3 混合气体通入氯化钡溶液中,出现浑浊是因为生成了BaSO4沉淀 | ||||
| B、SO2通入溴水中,溴水褪色,是因为SO2的漂白性 | ||||
C、反应2C+SiO2
| ||||
| D、在NaHCO3的溶液中滴加NaAlO2溶液中有白色沉淀生成,是因为二者发生完全水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中有一种物质被氧化,肯定有另一种物质被还原 |
| B、氧化反应和还原反应同时存在,缺一不可 |
| C、反应中有一种元素被氧化,肯定有另一种元素被还原 |
| D、元素处在最低价时只有还原性,最高价时只有氧化性,中间价态则性质稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:

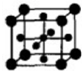
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L |
| B、0.9mol/L |
| C、1.8mol/L |
| D、1.9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com