
下列有关结构和性质的说法中,正确的是( )
A.分子中键长由小到大:HF<HCl<HBr<HI
B.分子中化学键的极性由小到大:HF<HCl<HBr<HI
C.碳元素的电负性小于氧元素,每个CO2分子中有4个σ键
D.Na、Mg、Al三种元素,其第一电离能由大到小的顺序为Na>Mg>Al
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
某有机物由C、H、O三种元素组成,它的红外吸收光谱表明有羟基O—H键和烃基上
C—H键的红外吸收光峰,且烃基与羟基上氢原子个数之比为2:1,该有机物可能为
A. 乙二醇 B. 乙醇 C. 甲醇 D. 丙三醇
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法中,不正确的是 ( )
A.淀粉、油脂、蛋白质在一定条件下都能发生水解反应
B.“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
C.除去乙酸乙酯中残留的乙酸、乙醇,可加过量饱和Na2CO3溶液振荡后,静置分液
D.淀粉遇碘酒变蓝色,葡萄糖能与新制Cu(OH)2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
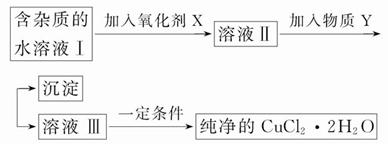
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)加入氧化剂的目的是 。
(2)最适合作氧化剂X的是 。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是 。
(4)若不用物质Y而是直接用碱能不能达到目的? (填“能”或“不能”)。若能,不用回答;若不能,试解释原因 。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作?
。
(6)若向溶液Ⅱ中加入碳酸钙,产生的现象是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
巴豆酸的结构简式为CH3—CH=CH—COOH。
试回答:
(1)巴豆酸的分子中含有 和 两种官能团(写名称)。
(2)巴豆酸与金属钠反应的化学方程式为
。
(3)巴豆酸 (选填“能”或“不能”)使溴水褪色。
(4)巴豆酸跟乙醇在浓硫酸催化下发生酯化反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质、结构的表述均正确,且存在因果关系的是( )
| 表述1 | 表述2 | |
| A | 晶体Si的熔点比I2的大 | 晶体Si中的化学键比I2的化学键强 |
| B | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
| C | 在形成化合物时,同一主族元素的化合价相同 | 同一主族元素原子的最外层电子数相同 |
| D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学习小组探究溴乙烷的消去反应并验证产物。
某学习小组探究溴乙烷的消去反应并验证产物。
实验原理:CH3CH2Br + NaOH 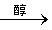 CH2=CH2↑ + NaBr + H2O
CH2=CH2↑ + NaBr + H2O
实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。
(1)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因: 。
(2)丙同学认为只要对实验装置进行适当改进,就可避免对乙烯气体检验的干扰,改进方法为: 。
改进实验装置后,再次进行实验,却又发现小试管中溶液颜色褪色不明显。该小组再次查阅资料,对实验进行进一步的改进。
资料一:溴乙烷于55℃时,在饱和氢氧化钠的乙醇溶液中发生取代反应的产物的百分比为99%,而消去反应产物仅为1%。
资料二:溴乙烷发生消去反应比较适宜的反应温度为90℃~110℃,在该范围,温度越高,产生乙烯的速率越快。
资料三:溴乙烷的沸点:38.2℃。
(3)结合资料一、二可知,丙同学改进实验装置后,溶液颜色褪色不明显的原因可能是 ,此时发生反应的化学方程式为: 。
(4)结合资料二、三,有同学认为应将实验装置中烧瓶改成三颈烧瓶并增加两种仪器,
这两种仪器是① 。 ② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要配制0.1 mol·L-1 CuSO4溶液480 mL。
按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、_______、________以及等质量的两片滤纸。
(2)计算,应选择下列正确________
A.需要CuSO4 固体8.0g B.需要CuSO4·5H2O晶体12.0 g
C.需要CuSO4·5H2O晶体12.5 g D.需要CuSO4固体7.7 g
(3)称量。所用砝码生锈则所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是_________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了_________________________________________。
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com