
����Ŀ����������Ҫ��������������ͭ�������г����Ľ�����
��1��Fe��Cu�������65%�����ᷴӦ���������NO2���÷�Ӧʹ�õ���������ʵ���Ũ��Ϊ______mol/L����֪��=1.4g/cm3����
��2����Ϊ0.1mol��Cu��Fe�������������ijŨ�ȵ����ᷴӦ����4.48L���壨��״���£�����÷�Ӧ���ĵ�����Ϊ______mol��
��3��4.4gFe��Cu���������������ᷴӦ���ų����������״���µ�1.12L��������Ϻ�ͨ��ˮ��ǡ�ñ���ȫ���գ�������ͭ������Ϊ______g��
��4��Fe��Cu����ﹲ��a mol������ͭ�����ʵ�������ΪX�����û����ȫ��Ͷ��b mol��������ʹ���ַ�Ӧ���ٶ�����Ļ�ԭ�������NO��
������Һ�н�������ֻ��Fe2+��Cu2+ʱ����b��ȡֵ��Χ��______����a��x��ʾ����
����x=0.2ʱ����ҺFe2+��Fe3+�����ʵ������ʱ���ڱ�״���²���NO 6.72L����a��b��ֵ����д����Ҫ�ļ�����̣�___________
���𰸡�14.44 0.7 1.6 ![]() ��b��
��b��![]() a��ֵΪ0.375��b��ֵΪ1.2
a��ֵΪ0.375��b��ֵΪ1.2
��������
(1)������Һ���������ʵ���Ũ�Ⱥ��������������Ļ����ϵ����õ���c=![]() ��
��
(2)ͭ�������������ᷴӦ����������ԭ��Ӧ�����ᱻ��ԭΪ�����������������Ϊ�����Σ����ݵ�Ԫ���غ����Ԫ������Һ��Ũ�ȣ�
(3)ͭ��������������ᷴӦ��������ͭ���������뵪�������������������������ˮ��Ӧ�������ᣬ�ݹ��������̣������ṩ�ĵ��ӵ���������õĵ��ӣ����ݶ������������ת���з��̼��㣮����m=nM����ͭ��������
(4)������Һ�еĽ�������ֻ��Fe2+��Cu2+ʱ��˵��Cuǡ����ȫ��Ӧ������ʣ�࣬��HNO3��Fe����ȫ��Ӧ�����������ʣ�࣬��Fe2+��ᱻ��һ������ΪFe3+�������Feʣ�࣬����Cu2+������Ӧ����HNO3��NO��N��3���ӣ��豻��ԭ��HNO3Ϊy mol���ܼƵ�3y mol���ӣ�Cu��Cu2+��Cuʧ2���ӣ���μӷ�Ӧ��CuΪz mol���ܼ�ʧ2z mol���ӣ�
Fe��Fe2+��Feʧ2���ӣ��μӷ�Ӧ��FeΪa(1��x)mol���ܼ�ʧ2a(1��x)mol���ӣ����ݵ�ʧ����������ȣ����ԣ�3y=2z+2a(1��x) ������Ӧ���������õ���������Fe(NO3��2��Cu(NO3)2�������������õ���������NO����NԪ���غ㣬�����У�y+2a(1��x)+2z=b �����������̣���ȥy���ɵ�b�ı���ʽ����a��x��z��ʾ�����μӷ�Ӧ��Cu�����ʵ���z��ȡֵ����0�����Ϊax������b�ı���ʽ���㣻
����x=0.2����Һ��Fe3+��Fe2+�����ʵ������ʱ��Cuȫ��Ϊͭ���ӣ����ݵ�ʧ�����غ�͵�ԭ���غ���㡣
(1)Fe��Cu�������65%�����ᷴӦ���������NO2���÷�Ӧʹ�õ���������ʵ���Ũ��=![]() =14.44mol/L��
=14.44mol/L��
(2)��Ϊ0.1mol��Cu��Fe�������������ijŨ�ȵ����ᷴӦ����4.48L���壨��״���£������ʵ���n=![]() =0.2mol��ͭ�������������ᷴӦ����������ԭ��Ӧ�����ᱻ��ԭΪ�����������������Ϊ�����Σ�Cu(NO3)2��Fe(NO3)3����Ԫ���غ���㣬��÷�Ӧ���ĵ��������ʵ���=0.1mol��2+0.1mol��3+0.2mol=0.7mol��
=0.2mol��ͭ�������������ᷴӦ����������ԭ��Ӧ�����ᱻ��ԭΪ�����������������Ϊ�����Σ�Cu(NO3)2��Fe(NO3)3����Ԫ���غ���㣬��÷�Ӧ���ĵ��������ʵ���=0.1mol��2+0.1mol��3+0.2mol=0.7mol��
(3)ͭ������������ᷴӦ��������ͭ�����������뵪�������������������������ˮ��Ӧ�������ᣬ�ݹ��������̣������ṩ�ĵ��ӵ���������õĵ��ӣ�n(O2)=![]() =0.05mol����Cu��Fe�����ʵ����ֱ�Ϊx��y�����������з��̣�x��64g/mol+y��56g/mol=4.4g���ݵ����غ��з��̣�2x+3��y=0.05mol��4����ã�x=0.025mol��y=0.05mol ��m(Cu)=0.025mol��64g/mol=1.6g��
=0.05mol����Cu��Fe�����ʵ����ֱ�Ϊx��y�����������з��̣�x��64g/mol+y��56g/mol=4.4g���ݵ����غ��з��̣�2x+3��y=0.05mol��4����ã�x=0.025mol��y=0.05mol ��m(Cu)=0.025mol��64g/mol=1.6g��
(4)������Һ�еĽ�������ֻ��Fe2+��Cu2+ʱ��˵��Cuǡ����ȫ��Ӧ������ʣ�࣬��HNO3��Fe����ȫ��Ӧ�����������ʣ�࣬��Fe2+��ᱻ��һ������ΪFe3+�������Feʣ�࣬����Cu2+������Ӧ����HNO3��NO��N��3���ӣ��豻��ԭ��HNO3Ϊy mol���ܼƵ�3y mol���ӣ�Cu��Cu2+��Cuʧ2���ӣ���μӷ�Ӧ��CuΪz mol���ܼ�ʧ2z mol���ӣ�Fe��Fe2+��Feʧ2���ӣ��μӷ�Ӧ��FeΪa(1��x)mol���ܼ�ʧ2a(1��x)mol���ӣ����ݵ�ʧ����������ȣ����ԣ�3y=2z+2a(1��x) ������Ӧ���������õ���������Fe(NO3)2��Cu(NO3)2�������������õ���������NO����NԪ���غ㣬�����У�y+2a(1��x)+2z=b �����������̣���ȥy��������b=8z+![]() �����μӷ�Ӧ��Cu�����ʵ���z��ȡֵ����0�����Ϊax���������У��ɵ�
�����μӷ�Ӧ��Cu�����ʵ���z��ȡֵ����0�����Ϊax���������У��ɵ�![]() ��b��
��b��![]() ��
��
����x=0.2����Һ��Fe3+��Fe2+�����ʵ������ʱ��Cuȫ��Ϊͭ���ӣ����Բμӷ�Ӧ��CuΪ0.2amol��Fe3+��Fe2+�����ʵ�����Ϊ0.4amol��HNO3��NO��N��3���ӣ�����6.72LNO���弴0.3mol���ܼƵ�0.9 mol���ӣ�Cu��Cu2+��Cuʧ2���ӣ���ʧ0.4a mol���ӣ�Fe��Fe2+��Feʧ2���ӣ���ʧ0.8amol���ӣ�Fe��Fe3+��Feʧ3���ӣ���ʧ1.2amol���ӣ����ݵ�ʧ����������ȣ����ԣ�0.9=0.4a+0.8a+1.2a�����a=0.375mol�����ݵ�ԭ���غ��֪��b=2n(Cu2+)+2n(Fe2+)+3n(Fe3+)+2n(NO)=2��0.2��0.375+2��0.4��0.375+3��0.4��0.375+0.3=1.2mol��


 ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д� Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������糧�ͷų���������������(NOx)��SO2��CO2���������ɻ������⡣��ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ġ�
(1)���������ü������ԭNOx��
CH4(g)��4NO2(g)==4NO(g)��CO2(g)��2H2O(g) ��H1����574 kJ/mol
CH4(g)��4NO(g)==2N2(g)��CO2(g)��2H2O(g) ��H2����1160 kJ/mol
д��CH4(g)��NO2(g)��Ӧ����N2(g)��CO2(g)��H2O(g)���Ȼ�ѧ����ʽ��_________________��
(2)��̼��
����һ���ں����ܱ������н�CO2ת��Ϊ�״���CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)
CH3OH(g)��H2O(g)
���������������ж��÷�Ӧ����ƽ��״̬����_________(����ĸ)��
A��2v��(H2)��v��(CH3OH) B��������������ܶȲ���
C��������ѹǿ���� D����Ӧ�����ͷ�����
����������һ������CO2������̼������ɱ���ܱ������з�Ӧ��C(s)��CO2(g)![]() 2CO(g) H�����ѹǿ���¶ȶ�CO���������[��(CO)��]��Ӱ����ͼ��ʾ���ش��������⣺
2CO(g) H�����ѹǿ���¶ȶ�CO���������[��(CO)��]��Ӱ����ͼ��ʾ���ش��������⣺

��ͼ��p1��p2��p3�Ĵ�С��ϵ��_________________��ͼ��a��b��c�����Ӧ��ƽ�ⳣ��Ka��Kb��Kc��С��ϵ��____________��
��900����1.013MPaʱ��1molCO2������̼��Ӧ��ƽ������������ΪV L��CO2��ת����Ϊ______(����һλС��)���÷�Ӧ��ƽ�ⳣ��K��_________��
����������NaOH��Һ����CO2��
����NaOH��Һ��ͨ��һ������CO2���壬������Һ��c(HCO32��):c(CO32��)=4:1����ʱ��Һ��pH=_______��(��֪�������£�H2CO3��K1=4��10��7��K2=5��10��11��lg2=0.3)
(3)����ȼú��������������̼����һ����������������Ӧ������(NH4)2SO4��(NH4)2SO4ˮ��Һ�����Ե�ԭ����_______________(�����ӷ���ʽ��ʾ)������ʱ����(NH4)2SO4��Һ�е���NaOH��Һ����Һ�����ԣ���������Һ����Ũ�ȴ�С��ϵc(Na��)____c(NH3��H2O)(��������������������=��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(SnSO4)�����Ȼ���(SnCl4)������ӡȾ�͵�ƹ�ҵ��ij�о�С������Ʊ�SnSO4��SnCl4·�����¡����������գ�
(һ)�Ʊ�SnSO4
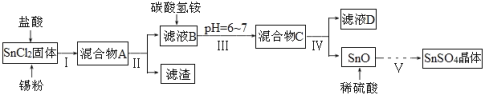
��֪�����������£�����ˮ��Һ����Sn2����Sn4��������Ҫ������ʽ��Sn2���ױ�������SnCl2����ˮ�⡣
(1)SnCl2������������ܵ�ԭ����_____________________��
(2)��������õ��IJ����������ձ����____________�����������Ҫϴ�ӹ���SnO�к��е����ʣ�����SnO�е�Cl-�Ƿ�ϴ�Ӹɾ��IJ���Ϊ______________��
(3)��������β���������Ũ����_________��_________��ϴ�ӡ����¸�����ɵõ����
(��)�Ʊ�SnCl4
ʵ���������ڵĽ���������﴿����������ȡ��ˮSnCl4(SnCl4�۵�-33�棬�е�114.1�棬����ʪ��������ˮ��)���˷�Ӧ���̷ų��������ȡ�ʵ��װ����ͼ��ʾ��

(4)����B������______________��
(5)ͼ��β������װ�ò������ƣ��Ľ��ķ����ǣ�________________(���Ի�ͼ��Ҳ���������ֱ�������ע���������Լ�������λ�õ�)��
(6)����Ӧ����ȥ����11.9 g����Ӧ������ƿ���ռ���23.8 g SnCl4����SnCl4�IJ���Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���Ʊ����跴Ӧ���Ȼ�ѧ����ʽ���£�SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)����H=+QkJ��mol-1(Q��0)��ij�¶ȡ�ѹǿ�£���һ������Ӧ��ͨ���ܱ������������Ϸ�Ӧ������������ȷ���ǣ� ��
Si(s)+4HCl(g)����H=+QkJ��mol-1(Q��0)��ij�¶ȡ�ѹǿ�£���һ������Ӧ��ͨ���ܱ������������Ϸ�Ӧ������������ȷ���ǣ� ��
A.��Ӧ�����У�������ѹǿ�����SiCl4��ת����
B.����Ӧ��ʼʱSiCl4Ϊ1mol�����ƽ��ʱ����������ΪQkJ
C.��Ӧ��4minʱ����HClŨ��Ϊ0.12mol��L-1����H2��Ӧ����Ϊ0.03mol��L-1��min-1
D.����Ӧ��������Ϊ0.025QkJʱ�����ɵ�HClͨ��100mL1mol��L-1��NaOH��Һǡ�÷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ȼ������гȻ���õ�廨��������ṹ��ʽ��ͼ�����ڸ��л������������ȷ����

�� ��Ni��������1mol���л������3mol H2�����ӳ���
�� ���л��ﲻ�ܷ���������Ӧ��
�� ���л������ʽΪC12H22O2��
�� ���л����ͬ���칹���в������з��ࣻ
�� 1 mol���л���ˮ��ʱֻ������1 mol NaOH
A. �ڢۢ� B. �٢ܢ� C. �ڢܢ� D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����N2O��NO��Ӧ����N2��NO2�������仯��ͼ��ʾ������˵��������ǣ� ��

A.ʹ�ô������Խ�����̬������
B.��Ӧ������������������������
C.��Ӧ���Ȼ�ѧ����ʽΪN2O(g)+NO(g)��N2(g)+NO2(g)+139kJ
D.ʹ�ô��������N2O��NO��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����FeCl3��ҺΪʵ�����̽�������������֮�䷴Ӧ�ĸ��Ӷ����ԡ�ʵ�����£�

(1)���з�Ӧ�����ӷ���ʽ��__________��
(2)�����ݳ�����ɫ������____________(д��ѧʽ)��
(3)���ڢ��е�ʵ������ͬѧ�������²⣬��������ʵ�飺
���飺ȡ���з�Ӧ����Һ����������ϡ�����ữ���ٵμ� BaCl2��Һ��������ɫ�������ó����ۣ�FeCl3�� Na2SO3 ������������ԭ��Ӧ�����ӷ���ʽ��_________��
���飺��Ϊ�����ʵ�鲻�Ͻ���������Ʋ�����ʵ�飬֤ʵ�˼���Ľ�������ȷ�ġ���ʵ�鷽����______��
(4)������ʵ���֪������˵����ȷ����___________ (����ĸ)��
a.����Ӧʱ���κͼ���������ˮ
b.����Һ���ܳ����ԡ����ԡ�����
c.�����η�Ӧʱ����һ��������������
d.�����η�Ӧʱ�������IJ�һ���Ǹ��ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ش���������
��1��ij�¶�ʱ�����pH��11��Ba(OH)2��ҺŨ����0.005mol��L��1��
�ٸ��¶���ˮ�����ӻ�����Kw��________��
���ڴ��¶��£���pH��12��Ba(OH)2��ҺVa L��pH��2������Vb L��ϡ������û��ҺΪ���ԣ���Va��Vb��________��
��2��25 ��ʱ���������ʵĵ���ƽ�ⳣ�����±���ʾ����ش��������⣺
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.8��10��5 | K1��4.3��10��7 K2��5.6��10��11 | 3.0��10��8 |
������˵����ȷ����__________
A��25 ��ʱ����CH3COOH��Һ�м���������NaOH��Һ��CH3COOH�ĵ���̶�������ƽ�ⳣ������
B��0.1molL-1 CH3COOH��Һ��ˮϡ�ͣ�ϡ�ͺ����Һ��ˮ�ĵ���̶ȼ�С
C��0.1molL-1 HClO��Һ��0.1molL-1 NaClO��Һ�������ϳ���Һ����
D��̼��������Һ������������Ŀ���
�� ͬŨ�ȵ�CH3COO����HCO��CO32-��ClO�����H����������ǿ������˳��Ϊ___
�� 25 ��ʱ��ijCH3COOH��CH3COOK�����Һ�����ԣ���û����Һ�У�![]() =________
=________
��3��úȼ���ŷŵ���������SO2��NO�����ü��Ե�NaClO2��Һ��Ϊ���ռ���ͬʱ���������������������ڹ��ݷ�Ӧ����ͨ�뺬��SO2��NO����������Ӧ�¶�Ϊ323 K��NaClO2��ҺŨ��Ϊ5��103mol��L1����Ӧ10min����Һ������Ũ�ȵķ���������±���
���� | SO42 | SO32 | NO3 | NO2 | Cl |
c/��mol��L1�� | 8.35��104 | 6.87��106 | 1.5��104 | 1.2��105 | 3.4��103 |
��д��NaClO2��Һ������������Ҫ��Ӧ�����ӷ���ʽ______��
���������Ca(ClO)2���NaClO2��������Ч������á��Դӻ�ѧƽ��ԭ��������Ca(ClO)2���NaClO2���е��ŵ���________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ���ǣ�������
A. ��������Һ��ͨ�������Ķ�����̼�������DZ��Ӻ�̼����
B. ����ͬϵ���У������Ͳ����Ӱ�죬ʹ�ö��߾��ױ�����
C. ![]() �ں˴Ź��������г�������壬����ԭ����֮��Ϊ3��2
�ں˴Ź��������г�������壬����ԭ����֮��Ϊ3��2
D. ����ȩ������ϩ�����е�����ԭ�ӿ��ܴ���ͬһƽ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com