
分析 (1)根据离子之间结合生成沉淀,不能共存,确定含有的两种物质;
(2)C与B的溶液混合时,产生红褐色沉淀和无色无味气体,沉淀为氢氧化铁、气体为二氧化碳;C与A的溶液混合时产生混合物沉淀,向该沉淀中滴入稀盐酸,沉淀部分溶解,最后留有白色沉淀不再溶解,则B为Na2CO3,A为Ba(OH)2,C为硫酸铁,另两种物质为氯化铝、硝酸镁或氯化镁、硝酸铝.
(3)由上面推断可知B为Na2CO3,碳酸根可与氢离子结合生成碳酸氢根;
(4)已知C为Fe2(SO4)3,A为Ba(OH)2,将0.02molA与0.01molC同时溶解在足量的蒸馏水中,反应生成碳酸钡沉淀和氢氧化铁沉淀,根据反应方程中的关系求出沉淀的量;
(5)将Cu投入D溶液中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,该气体为NO2,说明D中含有NO3-;
(6)D中含有NO3-,则E中含有Cl-,剩余Al3+、Mg2+,利用氢氧化铝溶液强碱的性质检验.
解答 解:(1)因Al3+、Mg2+、Fe3+和OH-反应生成沉淀,Al3+、Mg2+、Ba2+、Fe3+和CO32-反应,则不能共存,所以一定存在的物质为Na2CO3 和 Ba(OH)2,
故答案为:Na2CO3;Ba(OH)2;
(2)C与B的溶液混合时,产生红褐色沉淀和无色无味气体,沉淀为氢氧化铁、气体为二氧化碳;C与A的溶液混合时产生混合物沉淀,向该沉淀中滴入稀盐酸,沉淀部分溶解,最后留有白色沉淀不再溶解,则B为Na2CO3,A为Ba(OH)2,C为硫酸铁,另两种物质为氯化铝、硝酸镁或氯化镁、硝酸铝,因C为Fe2(SO4)3酸铁,则阴离子有SO42-,则X为SO42-,
故答案为:B;
(3)由上面推断可知B为Na2CO3,碳酸根可与氢离子结合生成碳酸氢根:CO32-+H+=HCO3-,故答案为:CO32-+H+=HCO3-;
(4)已知C为Fe2(SO4)3,A为Ba(OH)2,将0.02molA与0.01molC同时溶解在足量的蒸馏水中,反应生成碳酸钡沉淀和氢氧化铁沉淀,Fe2(SO4)3+3Ba(OH)2═2Fe(OH)3↓+3BaSO4↓,
根据方程可知,硫酸铁过量,按照Ba(OH)2计算,
则n(BaSO4)=0.02mol,n(Fe(OH)3)=$\frac{2}{3}$×0.02mol,
所以沉淀的质量为m(BaSO4)+m(Fe(OH)3)=0.02mol×233g/mol+$\frac{2}{3}$×0.02mol×107g/mol=6.09g
故答案为:6.09g;
(5)将Cu投入D溶液中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,该气体为NO2,说明D中含有NO3-,反应离子方程式为:3Cu+8H++2NO3-═3Cu2+2NO↑+4H2O,
故答案为:NO3-;3Cu+8H++2NO3-═3Cu2+2NO↑+4H2O;
(6)D中含有NO3-,则E中含有Cl-,剩余Al3+、Mg2+,Al(OH)3能溶于过量Ba(OH)2溶液,检验方案为:取少量D的溶液与试管中,逐渐进入Ba(OH)2溶液至过量,先出现白色沉淀后溶解,则D中含有Al3+,若生成的白色沉淀不溶解,则D中含有Mg2+,
故答案为:取少量D的溶液与试管中,逐渐进入Ba(OH)2溶液至过量,先出现白色沉淀后溶解,则D中含有Al3+,若生成的白色沉淀不溶解,则D中含有Mg2+.
点评 本题考查离子推断、实验方案设计等,是对所学知识的综合考查,题目难度较大,综合度较高,旨在考查学生的推断能力与方案设计能力,注意根据反应现象进行推断.


科目:高中化学 来源: 题型:选择题
| A. | 放电过程中电解质溶液中阴离子移向正极 | |
| B. | 放电时每转移0.5mol电子,负极有0.5molV2+被氧化 | |
| C. | 充电时阳极附近溶液的酸性减弱 | |
| D. | 充电时阳极反应式为:VO2++2H++e-═VO2++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都正确 | B. | ②③④⑤ | C. | ②③⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化石燃料属于可再生能源,不影响可持续发展 | |
| B. | 开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料 | |
| C. | 煤的气化技术在一定程度上实现了煤的高效、清洁利用 | |
| D. | 氢气燃烧热高,其燃烧产物是水,是一种理想的清洁燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
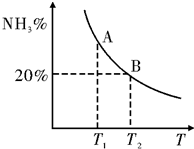 合成氨技术的发明使工业化人工固氮成为现实.
合成氨技术的发明使工业化人工固氮成为现实.| 温度/℃ CO2转化率% $\frac{n(N{H}_{3})}{n(C{O}_{2})}$ | 100 | 150 | 200 |
| 1 | 19.6 | 27.1 | 36.6 |
| 1.5 | a | b | c |
| 2 | d | e | f |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子晶体中,只存在离子键,不可能存在其它化学键 | |
| B. | 氧族元素(O、S、Se、Te)的氢化物的沸点依次升高 | |
| C. | NaHSO4、Na2O2晶体中的阴阳离子个数比均为1:1 | |
| D. | 晶体的硬度:金刚石>碳化硅>石英 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com