
| A. | 30% | B. | 37% | ||
| C. | 50% | D. | 数据不全无法计算 |
分析 3-甲基-2-戊烯分子式为C6H12,葡萄糖分子式为C6H12O6,丙酸分子式为C3H6O2,丁酸乙酯的分子式为C6H12O2,各物质中C、H原子的数目之比为1:2,故混合物中C、H元素质量之比为12:2=6:1,则根据H元素的质量分数可计算混合物中碳元素的质量分数,混合物中氧元素的质量分数=1-w(C)-w(H).
解答 解:3-甲基-2-戊烯分子式为C6H12,葡萄糖分子式为C6H12O6,丙酸分子式为C3H6O2,丁酸乙酯的分子式为C6H12O2,各物质中C、H原子的数目之比为1:2,故混合物中C、H元素质量之比为12:2=6:1,氢元素的质量分数为9%,则C元素质量分数为9%×6=54%,则混合物中氧元素的质量分数=1-54%-9%=37%,
故选:B.
点评 本题考查混合物中元素质量分数的计算,关键是根据分子式确定混合物中C、H元素的质量关系,较好的考查学生分析计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 已知C(s)+$\frac{ax}{0.02}$O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ | |
| C. | 已知反应X+Y=M+N为放热反应,故不必加热就可发生 | |
| D. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于57.3KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
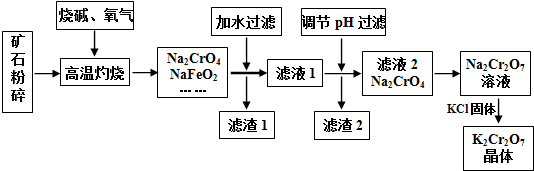
| 时间/(s) | 0 | 0.01 | 0.02 | 0.03 | 0.04 |
| (CrO42-)/(mol•L-1) | 0.20 | 1.6×10-2 | 1.2×10-2 | 1.0×10-2 | |
| (Cr2O72-)/(mol•L-1) | 0 | 9.2×10-2 | 9.4×10-2 | 9.5×10-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | Y |
| Z |
| A. | 四种元素的原子半径:r(Z)>r(X)>r(Y)>r(W) | |
| B. | 四种元素形成的单质最多有6种 | |
| C. | X与Y形成的气态化合物超过两种 | |
| D. | 四种元素中,Z的最高价氧化物对应的水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤⑥ | B. | ①③⑥ | C. | ②④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁元素基态原子的核外电子排布式是:1s22s22p63s2 | |
| B. | 铝元素原子核外共有5种不同运动状态的电子 | |
| C. | 钠元素离子半径比铝离子半径大 | |
| D. | 金属铝与钠的最高价氧化物的水化物溶液发生反应的离子方程式为2Al+2OH-+2H2O═2AlO${\;}_{2}^{-}$+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是水晶、玛瑙的主要成分,也是制造光导纤维的原料 | |
| B. | SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物 | |
| C. | 盛放NaOH溶液的试剂用橡皮塞,而不用玻璃塞 | |
| D. | Si是良好的半导体材料,是将太阳能转换为电能的常用材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油经分馏得到的各馏分仍然是多种烃的混合物 | |
| B. | 石油分馏的目的是将含碳原子数较多的烃先气化,经冷凝而分离出来 | |
| C. | 石油经过分馏、裂化等工序后得到大量乙烯、苯等不饱和烃 | |
| D. | 石油的炼制过程是将相对分子质量较大分子变成相对分子质量较小分子的过程 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com