
| A. | HBr | B. | H2S | C. | NH3 | D. | PH3 |
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 计算机芯片的主要材料是Si | |
| B. | 明矾能使海水淡化从而解决淡水危机 | |
| C. | 可用碘酒灭菌消毒是因为它能使蛋白质变性 | |
| D. | 钠、锶、钡等金属化合物可在燃放时呈现艳丽色彩 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
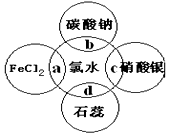 氯水中有多种成分,因而具有多重性质,根据氯水分别与如图四种物质发生的反应,填空a、b、c、d重合部分代表物质间反应,且氯水足量)
氯水中有多种成分,因而具有多重性质,根据氯水分别与如图四种物质发生的反应,填空a、b、c、d重合部分代表物质间反应,且氯水足量)查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中氮元素被氧化,氯元素被还原 | |
| B. | 还原性 NH4+>Cl- | |
| C. | 反应中每生成1 mol N2,转移6 mol电子 | |
| D. | 经此法处理过的废水可以直接排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46gNO2和N2O4混合气体中氮原子数为NA | |
| B. | 1mol 14C含有的中子数为6NA | |
| C. | 标准状况下,22.4LCCl4中含有的分子数为NA | |
| D. | 0.5molNa2O2与足量水反应,转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
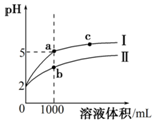 25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如图所示.下列说法不正确的是( )
25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如图所示.下列说法不正确的是( )| A. | 曲线I代表盐酸的稀释过程 | |
| B. | a溶液的导电性比c溶液的导电性强 | |
| C. | a溶液中和氢氧化钠的能力强于b溶液 | |
| D. | 将a、b两溶液加热至30℃,$\frac{c(C{l}^{-})}{c(C{H}_{3}CO{O}^{-})}$变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 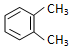 与 与 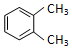 是同一种物质,说明苯分子中碳碳双键、碳碳单键交替排列 是同一种物质,说明苯分子中碳碳双键、碳碳单键交替排列 | |
| B. | 等质量的乙烯与乙醇充分燃烧时消耗氧气的质量相等 | |
| C. | 可用溴水鉴别汽油、四氯化碳和乙酸 | |
| D. | 苯和硝酸反应生成硝基苯与甲烷和氯气反应生成一氯甲烷的反应类型不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com