
【题目】一定温度下,在恒容密闭容器中发生反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)。下列能说明反应达到平衡状态的是
SO3(g)+NO(g)。下列能说明反应达到平衡状态的是
A. 体系的压强保持不变
B. 混合气体的密度保持不变
C. 混合气体的颜色保持不变
D. 每消耗1molSO3的同时生成1molNO2
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】用如图所示的装置及NaOH溶液、铁屑、稀H2SO4等试剂可以制得白色的Fe(OH)2沉淀。

(1)在试管Ⅰ里加入的试剂是____________________。
(2)在试管Ⅱ里加入的试剂是____________。
(3)为了制得白色Fe(OH)2沉淀,正确的操作顺序是______ (填下列序号)
①打开止水夹 ②检验试管Ⅱ出口处排出的H2的纯度 ③夹紧止水夹 ④在试管Ⅰ和Ⅱ中加入试剂,塞紧塞子
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是:_________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,可能存在的数据是( )
2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,可能存在的数据是( )
A. SO2为0.4 mol·L-1,O2为0.2 mol·L-1 B. SO2为0.2 mol·L-1
C. SO2、SO3分别为0.15 mol·L-1 、 0.3 mol·L-1 D. SO3为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂用以下几种方法处理SO2尾气。
(1)亚硫酸钠吸收法
① Na2SO3溶液吸收SO2的离子方程式为_______________;其产物的溶液中离子浓度由大到小的排列顺序为______________。
② 常温下,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是_______
(填序号)
a.c(Na+)+c(H+)>c(SO32-)+c(HSO3-)+c(OH-)
b.c(Na+)=c(SO32-)+c(HSO3-)+C(H2SO3)
c.c(Na+)>c(SO32-)>c(OH一)>c(H+)
d.水电离出c(OH一)=1×l0-8mol/L
③25 ℃时,H2SO3![]() HSO
HSO![]() +H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=______mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=______mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中![]() 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。
(2)电化学处理法
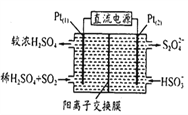
如图所示,Pt(1)电极的反应式为_________;碱性条件下,用Pt(2)电极排出的S2O42-溶液吸收NO2,使其转化为N2,同时有SO32-生成。若阳极转移电子6mol,则理论上处理NO2气体____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(6分)在稀氨水中存在平衡:NH3+H2O![]() NH
NH![]() +OH-,如进行下列操作,则NH3、NH
+OH-,如进行下列操作,则NH3、NH![]() 、H+、OH-浓度如何变化?请用“增大”“减小”“不变”填写。
、H+、OH-浓度如何变化?请用“增大”“减小”“不变”填写。
(1)通适量HCl气体时,c (NH3) ,c (H+) 。
(2)加入少量NaOH固体时,c(NH![]() ) ,c (OH-) 。
) ,c (OH-) 。
(3)加入NH4Cl晶体时,c (NH![]() ) ,c (OH-) 。
) ,c (OH-) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)向甲、乙两个均为1L的密闭容器中,分别充入5mol SO2和3mol O2,发生反应:2 SO2 (g)+O2 (g)![]() 2SO3(g) △H<0。甲容器在温度为T1的条件下反应,达到平衡时SO3的物质的量为4.5mol;乙容器在温度为T2的条件下反应,达到平衡时SO3的物质的量为4.6mol。则T1________T2(填“>”“<”),甲容器中反应的平衡常数K=___________。
2SO3(g) △H<0。甲容器在温度为T1的条件下反应,达到平衡时SO3的物质的量为4.5mol;乙容器在温度为T2的条件下反应,达到平衡时SO3的物质的量为4.6mol。则T1________T2(填“>”“<”),甲容器中反应的平衡常数K=___________。
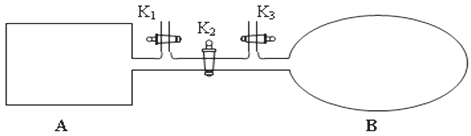
(2)如图所示,A是恒容的密闭容器,B是一个体积可变的充气气囊。保持恒温,关闭K2,分别将1 mol N2和3mol H2通过K1、K3充入A、B中,发生的反应为:
N2(g)+3H2(g) ![]() 2NH3(g),起始时A、B的体积相同均为1 L。
2NH3(g),起始时A、B的体积相同均为1 L。
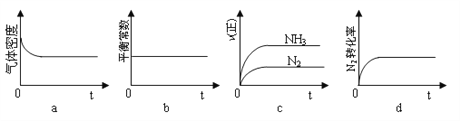
①下列示意图正确,且既能说明A容器中反应达到平衡状态,又能说明B容器中反应达到平衡状态的是_____。
②容器A中反应到达平衡时所需时间t s,达到平衡后容器的压强变为原来的5/6,则平均反应速率v(H2)=____。
(3)将0.1mol氨气分别通入1L pH=1的盐酸、硫酸和醋酸溶液中,完全反应后三溶液中NH4+离子浓度分别为c1、c2、c3,则三者浓度大小的关系为_______ (用c1、c2、c3和>、<、=表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是一种具有果香味的合成香料,下图为合成X的某种流程:

提示:①![]() 不能最终被氧化为-COOH;
不能最终被氧化为-COOH;
②D的产量可以用来衡量一个国家的石油化工水平。
请根据以上信息,回答下列问题:
(1)D与C分子中官能团的名称分别是____________,E的结构简式是____________。
(2)D→E的化学反应类型为____________反应。
(3)上述A、B、C、D、E、X六种物质中,互为同系物的是____________。
(4)反应C+E→X的化学方程式为___________________________________________。
(5)反应B→C的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了前20号元素中的某些元素性质的有关数据
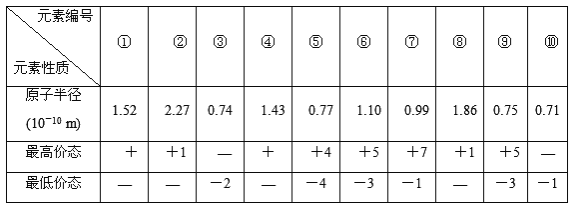
下列有关叙述正确的是
A. 以上10种元素的原子中,失去核外第一个电子所需能量最少的是⑧
B. 由⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是PCl5和CCl4
C. 某元素R的原子半径为1.02×10-10 m,该元素在周期表中位于第三周期第ⅤA族
D. 若物质Na2R3是一种含有非极性共价键的离子化合物,则其化合物的电子式![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com