
如下图装置(I)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池电的化学方程式为:
(II)为电解池的示意图。
当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是
A.电极A上发生的反应为:2S22---2e-=S42-
B.K+从右到左通过离子交换膜
C.电极X上发生的反应为:2Cl--2e-=Cl2↑
D.当有0.1mol K+通过离子交换膜,Y电极上产生2.24 L气体(标准状况)
科目:高中化学 来源:2012-2013学年广东省湛江市毕业班调研测试理综化学试卷(解析版) 题型:计算题
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4(g)+H2O(g) CO(g)+3H2(g)
△H=+206.0kJ•molˉ1
CO(g)+3H2(g)
△H=+206.0kJ•molˉ1
II:CO(g)+2H2(g) CH3OH(g)
△H=-129.0kJ•molˉ1
CH3OH(g)
△H=-129.0kJ•molˉ1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为 。
(2)将1.0mol CH4和1.0mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应I,测得在一定的压强下CH4的转化率与温度的关系如图。
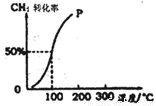
①假设100℃时达到平衡所需构时间为5min,则用H2表示该反应的平均反应速率为 。
②1000C时反应I的平衡常数为 。
(3)在压强为0.1 MPa、温度为300℃条件下,将a molCO与2a mol H2的混合气体在催化剂作用下发生反应II生成甲醇,平衡后将容器舶容积压缩到原来的1/2,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
A.平衡常数K增大 B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加 D.重新平衡c(H2)/c(CH3OH)减小
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将CO2+氧化成CO3+,然后以CO3+做氧化剂再把水中的甲醇氧化成CO2而净化。若下图装置中的电源为甲醇-空气-KOH溶液的燃料电池,则电池正极的电极反应式: ,该电池工作时,溶液中的OHˉ向 极移动。净化含1mol甲醇的水,燃料电池转移电子 mol。

查看答案和解析>>
科目:高中化学 来源:2011-2012年湖南湘潭等四县一中高一下学期期中联考化学试卷(解析版) 题型:实验题
某研究性学习小组设计了如下二组实验:
(I)实验验证元素周期律中, 非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。设计了如下图装置以验证氮、碳、硅元素的非金属性强弱。

设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:
A: ,B: ,C: 。
(2)写出烧杯中发生反应的离子方程式: 。
(Ⅱ )为比较Fe3+和Cu2+对H2O2的催化效果,甲、乙两位同学分别设计了如图一、图二所示的实验。
(1)图一可通过观察
定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是 ,或者将FeCl3 溶液改成物质的量浓度为 mol/L 的Fe2(SO4)3溶液。

(2)检查图二装置气密性的方法是 ;
图二所示实验中需测量的数据是 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年河南省辉县市高三上学期第四次月考理综化学卷 题型:选择题
如下图装置(I)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池电的化学方程式为:

(II)为电解池的示意图。

当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是
A.电极A上发生的反应为:2S22---2e-=S42-
B.K+从右到左通过离子交换膜
C.电极X上发生的反应为:2Cl--2e-=Cl2↑
D.当有0.1 mol K+通过离子交换膜,Y电极上产生2.24 L气体(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图装置(I)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池电的化学方程式为:
![]()
(II)为电解池的示意图。
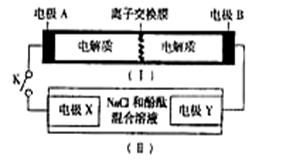
当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是
A.电极A上发生的反应为:2S22---2e-=S42-
B.K+从右到左通过离子交换膜
C.电极X上发生的反应为:2Cl--2e-=Cl2↑
D.当有0.1 mol K+通过离子交换膜,Y电极上产生2.24 L气体(标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com