
运用相关化学知识进行判断,下列结论错误的是( )
A.某吸热反应能自发进行,因此该反应是熵增反应
B.常温下, 0.1 mol/L氨水(电离度α=1%)的pH为11:
C.用蒸馏水润湿的试纸测溶液的pH,不一定会使结果偏低
D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
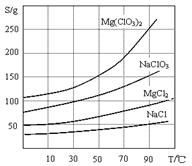
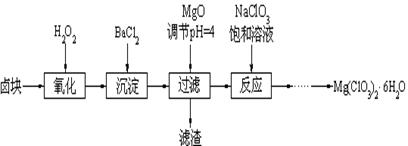
Mg(ClO3)2常用作催熟剂、除草剂等,下图为制备少量Mg(ClO3)2·6H2O的方法:
已知:1、卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
2、几种化合物的溶解度 (S)随温度(T)变化曲线如上图。
 (1)加入BaCl2的目的是除_________,如何判断该离子已除尽_____________________。
(1)加入BaCl2的目的是除_________,如何判断该离子已除尽_____________________。
(2)加入NaClO3饱和溶液会发生反应:MgCl2+2NaClO3==Mg(ClO3)2+2NaCl↓,请利用该反应,结合溶解度图,制取Mg(ClO3)2·6H2O的实验步骤依次为:
①取样,加入NaClO3饱和溶液充分反应;②蒸发浓缩;③ ;④冷却结晶;
⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50g产品溶解定容成100mL溶液。
步骤2:取10mL配好的溶液于锥形瓶中,加入10mL稀硫酸和20mL1.000mol/L的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100mol/L K2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:
Cr2O72-+6Fe2++14H+==2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL。
(3)写出步骤2中所发生反应的离子方程式 。
(4)步骤3中若滴定前用标准液润洗滴定管,会导致最终结果 (填“偏大”、“偏小”或“不变”)。
(5)产品中Mg(ClO3) 2·6H2O的质量分数为 (计算结果保留两位小数) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于乙烯和聚乙烯的叙述不正确的是 ( )
A.乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物
B.乙烯的化学性质比聚乙烯活泼
C.取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等
D.取等物质的量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的物质的量分别相等
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃组成的混合气体0.1mol, 完全燃烧得0.16molCO2和3.6g水。下列说法正确的是( )
A.混合气体一定没有甲烷 B.混合气体中一定是甲烷和乙烯
C.混合气体中一定没有乙烷 D.混合气体中一定有乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的的是 ( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.③④⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,对于可逆反应X(g)+3Y(g)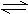 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A.c1的取值范围为0 mol·L-1<c1<0.14 mol·L-1
B.平衡时,Y和Z的生成速率之比为2∶3
C.X、Y的转化率不相等 D.c1∶c2=3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:强酸和强碱在稀溶液中发生反应时的中和热为57.3 kJ · mol-1,101 k Pa时辛烷的燃烧热为5518 kJ·mol-1。则下列热化学方程式书写正确的是( )
A.H++OH-=H2O △H = -57.3kJ·mol-1
B.2NaOH(aq)+ H2SO4(aq)= Na2SO4(aq)+2H2O(l) △H = -114.6 kJ·mol-1
C.2C8H18(l) + 25O2(g) = 16CO2(g)+18H2O(g) △H = -11036 kJ·mol-1
D.2C8H18(l) + 25O2(g) = 16CO2(g)+18H2O(l) △H = -5518kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
人体血液里存在重要的酸碱平衡: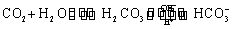 使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随
使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随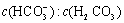 变化关系如下表:
变化关系如下表:
|
| 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.4 | 7.45 |
下列说法不正确的是( )
A.正常人体血液中,HCO3-的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)<c(HCO3-)
D.pH=7.40的血液中,HCO3-的水解程度一定大于H2CO3的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
巴豆酸的结构简式为CH3CH=CHCOOH 现有:①氯化氢,②溴水, ③纯碱溶液,④酸性KMnO4溶液, ⑤乙醇,试根据其结构特点,判断在一定条件下能与巴豆酸反应的物质组合是
A.只有②④⑤ B.只有①③④ C.只有①②③ D.都可以
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com