
| 共价键 | C-C | C═C | C-H | H-H |
| 键能/(kJ•mol-1) | 348 | 610 | 413 | 436 |
 (g)+3H2(g)→
(g)+3H2(g)→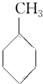 (g)的反应热;
(g)的反应热;| A. | ①②③④ | B. | ③④⑤ | C. | ④⑤ | D. | ⑥ |
分析 ①燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,氢气燃烧生成液态水;
②能量越高越不稳定;
③一定条件下,反应热与平衡移动无关,与化学计量数与物质的状态有关;
④苯环中不存在碳碳双键;
⑤金刚石与石墨的结构不同,能量不相同;
⑥燃烧热指:25℃,101kPa时1mol物质完全燃烧生成稳定氧化物放出的热量.
解答 解:①燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,氢气燃烧生成液态水,由热化学方程式可知,氢气的燃烧热<-241.8kJ•mol-1,故错误;
②单质A转化为单质B是一个吸热过程,则B的能量比A的高,能量越高越不稳定,故错误;
③一定条件下,反应热与平衡移动无关,与化学计量数与物质的状态有关,故错误;
④反应热=反应物总键能-生成物总键能,由于苯环中不存在碳碳双键,不能计算反应热,故错误;
⑤金刚石与石墨的结构不同,能量不相同,在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量不相等,故错误;
⑥碳的燃烧热指:25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量,故正确,
故选D.
点评 本题考查燃烧热、反应热有关计算、热化学方程式等,注意对概念与热化学方程式的理解,注意③中平衡移动,放出的热量发生变化,但热化学方程式焓变不变.


科目:高中化学 来源: 题型:选择题
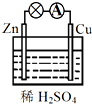
| A. | Cu为正极,SO42+向正极移动 | B. | 电子由铜片通过导线流向锌片 | ||
| C. | 该装置能将电能转化为化学能 | D. | 正极反应为 2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
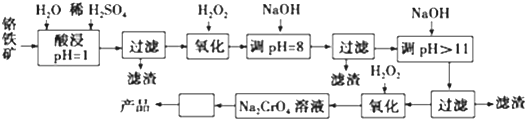
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | 9.0 | -- | -- |
| 沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8 | 9(>9溶解) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
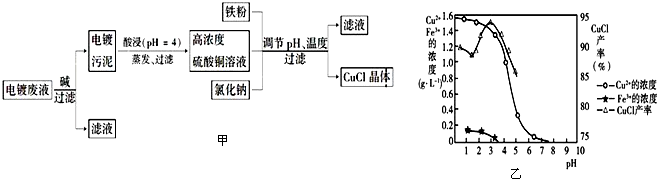
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFeI2与足量氯气反应时转移的电子数为3NA | |
| B. | 1L2mol•L-1 K2S溶液中S2-和HS-的总数为2NA | |
| C. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| D. | 50mL18mol•L-1浓硫酸与足量铜微热反应,转移的电子数为1.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
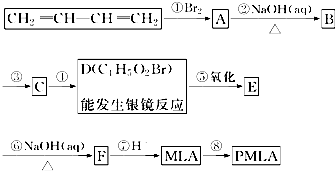
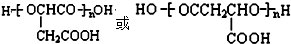 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
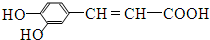 .下列有关咖啡酸的说法中,不正确的是( )
.下列有关咖啡酸的说法中,不正确的是( )| A. | 咖啡酸分子中的所有原子不可能共平面 | |
| B. | 咖啡酸可以发生还原、酯化、加聚、显色等反应 | |
| C. | 1mol咖啡酸可与4 mol Br2发生反应 | |
| D. | 1mol咖啡酸与NaOH溶液反应最多消耗1mol的NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雷雨天气时空气中能生成少量的氮氧化物,属于氮的固定 | |
| B. | 实验室用氯化铵溶液和氢氧化钙溶液混合制取氨气 | |
| C. | 铵盐化学性质都很稳定 | |
| D. | O2、NO、NO2都能用浓硫酸干燥,且通常情况下能共存 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com