
| ¶ž¼×±½Ņ»äåĖ®“śĪļČŪµć£Ø”ę£© | 234 | 206 | 213.8 | 204 | 211.5 | 205 |
| ¶ŌÓ¦¶ž¼×±½ČŪµć£Ø”ę£© | 13.3 | -47.9 | -25.2 | -47.9 | -25.2 | -47.9 |
| A£® | ČŪµć234”ęµÄŅ»ä嶞¼×±½ŹĒŅ»äå¶Ō¶ž¼×±½ | |
| B£® | ČŪµć204”ęµÄŅ»ä嶞¼×±½ŹĒŅ»äåĮŚ¶ž¼×±½ | |
| C£® | ČŪµć-47.9”ęµÄ¶ž¼×±½ŹĒ¶Ō¶ž¼×±½ | |
| D£® | ČŪµć205”ęµÄŅ»ä嶞¼×±½ŹĒŅ»äå¼ä¶ž¼×±½ |
·ÖĪö ¶ž¼×±½ÓŠČżÖÖĶ¬·ÖŅģ¹¹Ģ壬·Ö±šĪŖ¶Ō¶ž¼×±½”¢¼ä¶ž¼×±½ŗĶĮŚ¶ž¼×±½£®ĘäŅ»äå“śĪļ·Ö±šÓŠ1ÖÖ”¢3ÖÖŗĶ2ÖÖ£®øł¾Ż±ķÖŠ¶ŌÓ¦¶ž¼×±½µÄČŪµćæÉÅŠ¶Ļ£¬ČŪµćĪŖ13.3”ęµÄ¶ž¼×±½Ö»ÓŠŅ»ÖÖŅ»äå“śĪļ£¬ČŪµćĪŖ-47.9”ęµÄ¶ž¼×±½ÓŠ3ÖÖŅ»äå“śĪļ£¬¶ųČŪµćĪŖ-25.2”ęµÄ¶ž¼×±½ÓŠ2ÖÖŅ»äå“śĪļ£®Ņņ“ĖČŪµćĪŖ13.3”ęµÄ¶ž¼×±½ŹĒ¶Ō¶ž¼×±½£¬ČŪµćĪŖ-47.9”ęµÄ¶ž¼×±½ŹĒ¼ä¶ž¼×±½£¬ČŪµćĪŖ-25.2”ęµÄ¶ž¼×±½ŹĒĮŚ¶ž¼×±½£¬¾Ż“ĖŃ”Ōń¼“æÉ£®
½ā“š ½ā£ŗ¶ž¼×±½ÓŠČżÖÖĶ¬·ÖŅģ¹¹Ģ壬·Ö±šĪŖ¶Ō¶ž¼×±½”¢¼ä¶ž¼×±½ŗĶĮŚ¶ž¼×±½£®ĘäŅ»äå“śĪļ·Ö±šÓŠ1ÖÖ”¢3ÖÖŗĶ2ÖÖ£®øł¾Ż±ķÖŠ¶ŌÓ¦¶ž¼×±½µÄČŪµćæÉÅŠ¶Ļ£¬ČŪµćĪŖ13.3”ęµÄ¶ž¼×±½Ö»ÓŠŅ»ÖÖŅ»äå“śĪļ£¬ČŪµćĪŖ-47.9”ęµÄ¶ž¼×±½ÓŠ3ÖÖŅ»äå“śĪļ£¬¶ųČŪµćĪŖ-25.2”ęµÄ¶ž¼×±½ÓŠ2ÖÖŅ»äå“śĪļ£®Ņņ“ĖČŪµćĪŖ13.3”ęµÄ¶ž¼×±½ŹĒ¶Ō¶ž¼×±½£¬ČŪµćĪŖ-47.9”ęµÄ¶ž¼×±½ŹĒ¼ä¶ž¼×±½£¬ČŪµćĪŖ-25.2”ęµÄ¶ž¼×±½ŹĒĮŚ¶ž¼×±½£¬
A£®ČŪµćĪŖ234”ęµÄŹĒŅ»äå“ś¶Ō¶ž¼×±½£¬¹ŹAÕżČ·£»
B£®ČŪµćĪŖ204”ęµÄŹĒŅ»äå“ś¼ä¶ž¼×±½£¬¹ŹB“ķĪó£»
C£®ČŪµć-47.9”ęµÄ¶ž¼×±½ŹĒ¼ä¶ž¼×±½£¬¹ŹC“ķĪó£»
D£®ČŪµć205”ęµÄŅ»ä嶞¼×±½ŹĒŅ»äå¼ä¶ž¼×±½£¬¹ŹDÕżČ·£»
¹ŹŃ”AD£®
µćĘĄ ±¾Ģāæ¼²éĶ¬·ÖŅģ¹¹Ģ唢ӊ»śĪļµÄĶʶĻµČ£¬ÄѶČÖŠµČ£¬øł¾Ż±ķÖŠŹż¾ŻÅŠ¶ĻĶ¬·ÖŅģ¹¹ĢåµÄŅ»äå“śĪļ·ŠµćŹĒ½āĢāµÄ¹Ų¼ü£¬²ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¶Ō»ł“”ÖŖŹ¶µÄÓ¦ÓĆÄÜĮ¦£®£®


 ³ö²ŹĶ¬²½“óŹŌ¾ķĻµĮŠ“š°ø
³ö²ŹĶ¬²½“óŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬2.24 LC2H4ŗĶC2H2µÄ»ģŗĻĘųĢåÖŠŗ¬Ģ¼Ō×ÓŹżÄæŠ”ÓŚ0.2 NA | |
| B£® | 100 mL 1.0 mol/L FeCl3ČÜŅŗÓė×ćĮæCu·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.2 NA | |
| C£® | ±źæöĻĀ44.8 mLĀČĘųĶØČė×ćĮæĖ®ÖŠ·¢Éś·“Ó¦£¬×ŖŅʵē×ÓŹżĪŖ2”Į10-3NA | |
| D£® | ³£ĪĀĻĀ£¬pH=2µÄH2SO4ČÜŅŗÖŠŗ¬ÓŠµÄH+ŹżÄæĪŖ0.02 NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
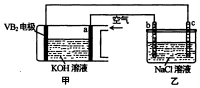 ¼īŠŌÅš»Æ·°--æÕĘųµē³Ų¹¤×÷Ź±·“Ó¦ĪŖ£ŗ4VB2+11O2=4B2O3+2V2O5£¬ŹŅĪĀĻĀÓĆøƵē³ŲĪŖµēŌ“£¬ÓƶčŠŌµē¼«µē½ā±„ŗĶĀČ»ÆÄĘČÜŅŗ£¬×°ÖĆČēĶ¼£®µ±ĶāµēĀ·ÖŠĶعż0.04molµē×ÓŹ±£¬ŅŅ×°ÖĆÖŠČÜŅŗµÄĢå»żĪŖ400mL£®ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
¼īŠŌÅš»Æ·°--æÕĘųµē³Ų¹¤×÷Ź±·“Ó¦ĪŖ£ŗ4VB2+11O2=4B2O3+2V2O5£¬ŹŅĪĀĻĀÓĆøƵē³ŲĪŖµēŌ“£¬ÓƶčŠŌµē¼«µē½ā±„ŗĶĀČ»ÆÄĘČÜŅŗ£¬×°ÖĆČēĶ¼£®µ±ĶāµēĀ·ÖŠĶعż0.04molµē×ÓŹ±£¬ŅŅ×°ÖĆÖŠČÜŅŗµÄĢå»żĪŖ400mL£®ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ĶāµēĀ·ÖŠµē×ÓÓÉaµē¼«Į÷Ļņbµē¼« | |
| B£® | µē¼«ÉĻÉś³ÉĘųĢåµÄĢå»żĪŖ4.48L | |
| C£® | ŅŅ×°ÖĆÖŠČÜŅŗµÄpHĪŖ13 | |
| D£® | VB2µē¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ£ŗVB2+11H2O-22e-=VB2+2B2O3+22H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 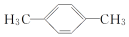 | B£® | 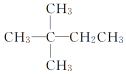 | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4ÖÖ | B£® | 5ÖÖ | C£® | 6ÖÖ | D£® | 7ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6ÖÖ | B£® | 7ÖÖ | C£® | 8ÖÖ | D£® | 9ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cl2ŹĒŃõ»Æ¼Į£¬NaOHŹĒ»¹Ō¼Į | |
| B£® | ĆæÉś³É1 mol NaClO3×ŖŅĘ6 molµē×Ó | |
| C£® | »¹Ō²śĪļŹĒNaClO3£¬Ńõ»Æ²śĪļŹĒNaCl | |
| D£® | ±»Ńõ»ÆµÄĀČŌ×ÓÓė±»»¹ŌµÄĀČŌ×ÓøöŹż±ČĪŖ1£ŗ5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
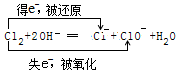 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com