
| A. | ①②⑤ | B. | ③④ | C. | ①②④ | D. | ①③ |
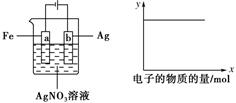
分析 根据图知,该装置为电镀池,阳极上电极反应式为Ag-e-=Ag+、阴极电极反应式为Ag++e-=Ag,阳极上金属分解、阴极上金属析出,且阳极溶解金属的质量等于阴极析出金属质量,则相当于电解质溶液不发生反应,据此分析解答.
解答 解:根据图知,该装置为电镀池,阳极上电极反应式为Ag-e-=Ag+、阴极电极反应式为Ag++e-=Ag,阳极上金属分解、阴极上金属析出,且阳极溶解金属的质量等于阴极析出金属质量,则相当于电解质溶液不发生反应,所以①②⑤这三个物理量都不变,a电极质量增加、b电极质量减少,
故选A.
点评 本题考查电镀,为高频考点,明确电镀池特点是解本题关键,知道电镀时相当于电解质溶液不参加反应即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用瓷坩埚熔融氢氧化钠或碳酸钠 | |
| B. | 用玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液的pH值 | |
| C. | 用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 | |
| D. | 读取量筒内溶液液体的体积,俯视读数导致读数偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
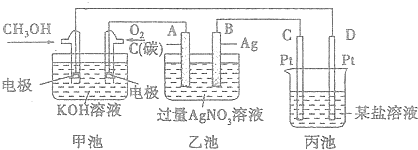
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝是地壳中含量最多的金属元素 | |
| B. | 铝单质能与盐酸溶液反应,又能与NaOH溶液反应 | |
| C. | 在常温下,铝不能和氧气反应 | |
| D. | 在化学反应中,铝容易失去电子,是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{100w}{w+18a}$% | B. | $\frac{7100w}{161(w+18a)}$% | C. | $\frac{100w}{w+36a}$% | D. | $\frac{7100w}{161(w+36a)}$% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定性检验C2H5Cl中的氯元素:将C2H5Cl和NaOH溶液混合加热后,再加AgNO3溶液 | |
| B. | 检验汽油是否含有烯烃:取少量汽油,加入碘酒,振荡并观察 | |
| C. | 制乙烯:将无水乙醇加热到170℃ | |
| D. | 蛋白质变性实验:将硫酸铜溶液滴入鸡蛋清溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡有能量变化的过程都是化学变化 | |
| B. | 吸热反应只有在加热的条件下才能进行 | |
| C. | 放热反应可能需要在加热的条件下才能进行 | |
| D. | 化学反应中的能量变化都只以热能的形式表现出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
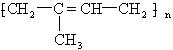 某有机化合物能在一定条件下发生加聚反应,生成高分子有机物,其结构简式如图,则合成该高聚物的单体是( )
某有机化合物能在一定条件下发生加聚反应,生成高分子有机物,其结构简式如图,则合成该高聚物的单体是( )| A. | 2-甲基-2-丁烯 | B. | 乙烯和丙烯 | ||
| C. | 1,3-T二烯 | D. | 2-甲基-1,3-丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
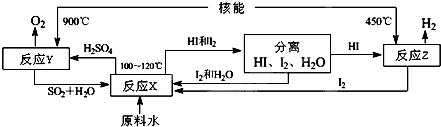
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com