
| A. | 除③外 | B. | 只有①⑤⑥⑧ | C. | 除③⑧外 | D. | 除③④⑦⑧ |
分析 具有正四面体结构的物质中,中心原子价层电子对个数是4,且不含孤电子对,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.
解答 解:①白磷分子的结构为: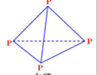 ,P原子价层电子对个数=$\frac{5-1×3}{2}$=4,为sp3杂化,所以空间构型是正四面体构型,故①正确;
,P原子价层电子对个数=$\frac{5-1×3}{2}$=4,为sp3杂化,所以空间构型是正四面体构型,故①正确;
②金刚石的结构为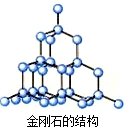 ,金刚石中碳原子与四个碳原子形成4个共价单键,碳原子的杂化类型为sp3杂化,为正四面体结构,故②正确;
,金刚石中碳原子与四个碳原子形成4个共价单键,碳原子的杂化类型为sp3杂化,为正四面体结构,故②正确;
③二氧化碳的结构为O=C=O,分子中碳原子含有2个σ键且不含孤电子对,采用sp杂化,其空间构型是直线形,不存在正四面体结构,故③错误;
④SiO2晶体结构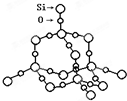 ,二氧化硅晶体中存在四面体结构单元,每个硅原子能构成四个共价键,每个氧原子能形成2个共价键,Si处于中心,O处于4个顶角,为sp3杂化,存在正四面体结构,故④正确;
,二氧化硅晶体中存在四面体结构单元,每个硅原子能构成四个共价键,每个氧原子能形成2个共价键,Si处于中心,O处于4个顶角,为sp3杂化,存在正四面体结构,故④正确;
⑤CH4分子中心原子价层电子对个数=4$\frac{4-1×4}{2}$=4,中心原子为sp3杂化,4个共价键完全相同,则其分子结构为四面体结构,故⑤正确;
⑥四氯化碳中,碳原子与四个氯原子形成4个σ键,中心原子价层电子对个数=4$\frac{4-1×4}{2}$=4,中心原子为sp3杂化,所以其空间构型为正四面体,故⑥正确;
⑦晶体硅的空间结构与金刚石的相似,为空间四面体结构,中心原子为sp3杂化,4个共价键完全相同,为正四面体,故⑦正确;
⑧NH4+中中心原子价层电子对个数=4$\frac{5-1-1×4}{2}$=4,中心原子为sp3杂化,为四面体结构,4个共价键完全相同,为正四面体,故⑧正确;
所以除③外都正确,
故选A.
点评 本题考查了晶体的结构,注意把握价层电子对互斥理论的应用,明确晶体结构是解此题关键,注意正四面体结构的物质,中心原子为sp3杂化,结构对称,题目难度中等.


 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:3 | B. | 1:4 | C. | 1:5 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CuCl2(无水CuSO4) | B. | NaOH(H2O) | C. | NaCl(HCl气体) | D. | CuSO4(Cu(OH)2固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温、低压 | B. | 低温、高压 | C. | 低温、低压 | D. | 高温、高压 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
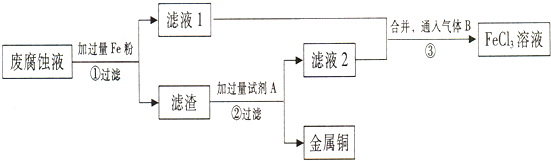
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5Cl | B. | C2H4Cl2 | C. | C2H6 | D. | C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于20 mL | B. | 等于30 mL | C. | 大于30 mL | D. | 小于20 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com