
| A. | F2 | B. | H2O | C. | PCl3 | D. | SO2 |
分析 如果化合物中元素的最外层电子数+化合价的绝对值=8,则该元素满足8电子稳定结构,否则不是,据此对各选项进行判断.
解答 解:A.F2中N原子最外层7个电子,N原子形成1个共价键,每个共价键提供一个电子,所以每个F原子周围电子数为:7+1=8,故A正确;
B.水分子中,氢原子最外层有2个电子,所以氢原子不满足8电子稳定结构,故B错误;
C.PCl3中P元素化合价为+3,P原子最外层电子数为5,所以3+5=8,P原子满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,成键原子不同共用电子对会发生偏移,故C正确;
D.SO2分子中,S原子的最外层含有6个电子,S的化合价为+4,则二氧化硫分子中S的最外层电子数为:6+4=10,故D错误;
故选AC.
点评 本题考查原子核外电子排布,题目难度不大,注意根据“化合物中元素的最外层电子数+化合价的绝对值=8,则该元素满足8电子稳定结构”分析,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 配制1.00mol/LNaCl溶液时,将称好的NaCl固体直接放入容量瓶中溶解 | |
| B. | 蒸馏时,冷却水从冷凝管的下口通入,上口流出 | |
| C. | 用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出 | |
| D. | 用四氯化碳萃取碘水中的碘单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 )
) .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将CO2溶于水中 | B. | Na2O2溶于水中 | C. | 将SO3溶于水中 | D. | NaHSO4溶于水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
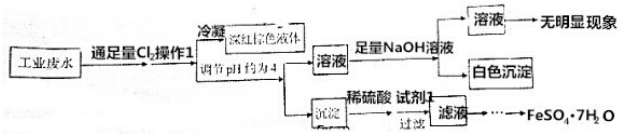
| A. | 该工业废水中肯定存在Cu2+、I- | |
| B. | 若废水中存在NO3-,则肯定存在Fe3+ | |
| C. | 操作1为鼓入热空气,试剂1为Fe | |
| D. | 为了得到FeSO4•7H2O,需要经过蒸发浓缩、冷却结晶,过滤、洗涤、干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | 2FeO+Si$\frac{\underline{\;高温\;}}{\;}$2Fe+SiO2 | ||
| C. | SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑ | D. | CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+ | H+ | Ba2+ |
| 阴离子 | OH- | CO32- | SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com