
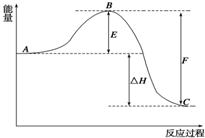
 2SO2��g��+O2��g��?2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g������Ϊ1mol SO3��g���ġ�H1=-98.32kJ?mol-1
2SO2��g��+O2��g��?2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g������Ϊ1mol SO3��g���ġ�H1=-98.32kJ?mol-1


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 A��B��C��Ϊ������Ԫ�أ����������ڱ��е�λ����ͼ����֪B��C��Ԫ�������ڱ���������֮����AԪ����������2����B��CԪ�ص�ԭ������֮����AԪ��ԭ��������4������A��B��C�ֱ��ǣ�������
A��B��C��Ϊ������Ԫ�أ����������ڱ��е�λ����ͼ����֪B��C��Ԫ�������ڱ���������֮����AԪ����������2����B��CԪ�ص�ԭ������֮����AԪ��ԭ��������4������A��B��C�ֱ��ǣ�������| A��Be Na Al |
| B��B Mg Si |
| C��O P Cl |
| D��C Al P |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
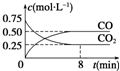 һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g����H��0��1 100��ʱ����ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2�����CO�����Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g����H��0��1 100��ʱ����ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2�����CO�����Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��| ���� | �� | �� |
| ��Ӧ��Ͷ���� | 3mol Fe�� 2mol CO2 | 4mol FeO�� 3mol CO |
| CO��Ũ�ȣ�mol?L-1�� | c1 | c2 |
| CO2��������� | ��1 | ��2 |
| ��ϵѹǿ��Pa�� | p1 | p2 |
| ��̬��Ӧ���ת���� | ��1 | ��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| T��K�� | K1 | K2 |
| 973 | 1.47 | 2.36 |
| 1173 | 2.15 | 1.67 |

| ��ѧʽ | ����ƽ�ⳣ����25�棩 |
| HCN | K=4.9��10-10 |
| CH3COOH | K=1.8��10-5 |
| H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ѧ��Ӧ | ƽ�ⳣ�� | �¶� | |
| 973K | 1173K | ||
| ��Fe��s��+CO2��g��?FeO��s��+CO��g�� | K1 | 1.47 | 2.15 |
| ��Fe��s��+H2O��g��?FeO��s��+H2��g�� | K2 | 2.38 | 1.67 |
| ��CO��g��+H2O��g��?CO2��g��+H2��g�� | K3 | �� | �� |
| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| �� | �� | �� | �� | |||||
| �� | �� | �� | �� | �� | �� | |||
| �� | �� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��˫��ˮ | B��ʳ�� |
| C�������� | D���������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com