
分析下表中各项的排布规律,有机物X是按此规律排布的第23项,下列有关X的组成、性质的说法中肯定错误的是
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | CH2O | CH2O2 | CH4O | C2H6 | C2H4O | C2H4O2 | C2H6O |
①是己酸 ②是己醇 ③是戊酸甲酯 ④在稀硫酸中易变质 ⑤一定能与钠反应
A.②⑤ B.①③④
C.③④ D.②③⑤
科目:高中化学 来源: 题型:
在相同的温度和压强下,二氧化氮和二氧化碳两种气体的分子数相同,则下列它们的( )一定相同。
(1)体积(2)所含原子个数 (3)物质的量(4)质量 (5)密度
A.只有(1)(2)(3) B.只有(1)(2)(4)
C.只有(2)(3)(5) D.(1)(2)(3)(4)(5)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:将Cl2通入适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且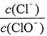
的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
A.若某温度下,反应后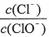 =11,则溶液中
=11,则溶液中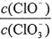 =
=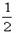
B.参加反应的氯气的物质的量等于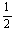 a mol
a mol
C.改变温度,反应中转移电子的物质的量ne的范围: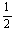 a mol≤ne≤
a mol≤ne≤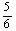 a mol
a mol
D.改变温度,产物中KC1O3的最大理论产量为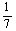 a mol
a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分散系,不会产生丁达尔效应的是 ( )
①鸡蛋清 ②淀粉溶液 ③硫酸钠溶液 ④Fe(OH)3胶体 ⑤Fe(OH)3悬浊液
A.①③ B.②③⑤ C.③④⑤ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用密度为1.19g/mL,质量分数为36.5% 浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液
| 应量取盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ________。
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2—3cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是
(4)若出现如下情况,对所配溶液浓度将有何影响(填偏高、偏低或无影响)?
没有进行A操作 ;
加蒸馏水时不慎超过了刻度 ;
定容时俯视_________________________;
未将溶液冷却就转入了容量瓶 ;
(5)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度线应 。
查看答案和解析>>
科目:高中化学 来源: 题型:
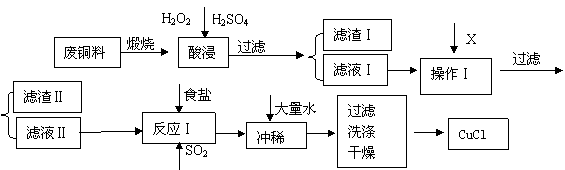
CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 5.6 | 6.7 |
| Al(OH)3 | 3.8 | 4.7 |
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀。
(1)煅烧的主要目的是: 。
(2)操作Ⅰ为调节溶液的PH值,范围为 ,加入的物质X可以是( )
A、CuO B、Cu(OH)2 C、NaOH 溶液 D、CaCO3
(3)滤渣Ⅱ的主要成分是 。
(4)往滤液Ⅱ中加入食盐并通入SO2可生成CuCl2-,请写出反应的离子方程式:
。
(5)在反应Ⅰ中,温度控制在70~80℃并使用浓NaCl溶液,主要目的是: 。
(6)常温下,已知CuOH的KSP为1.0×10-14,则Cu++H2O  CuOH + H+的平衡常数为: 。
CuOH + H+的平衡常数为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中元素均为中学化学中常见短周期元素,根据表中信息,下列说法不正确的是
| 元素代号 | X | Y | Z | W | N |
| 原子半径/nm | 0.186 | 0.074 | 0.102 | 0.099 | 0.160 |
| 主要化合价 | +1 | -2 | -2、+6 | +7、-1 | +2 |
A.常温下单质与水反应速率:X > N
B.最高价氧化物对应水化物酸性:W > Z
C.X 与W形成的化合物是共价化合物
D.X和Y的单质在一定条件下反应可生成一种淡黄色的固体化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某化学反应的平衡常数表达式为K=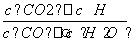 ,在不同的温度下该反应的平衡常数值分别为:
,在不同的温度下该反应的平衡常数值分别为:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述不正确的是
A.该反应的化学方程式是:CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830 ℃,此时测得CO为0.4 mol时,该反应为平衡状态
D.某温度下,如果平衡浓度符合下列关系式: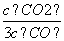 =
=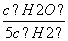 ,判断此时的温度是1000 ℃
,判断此时的温度是1000 ℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com