
【题目】根据下图判断,下列说法正确的是( )
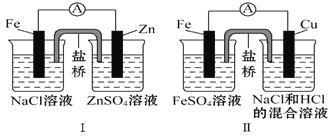
A. 装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-Fe2+
B. 装置Ⅰ和装置Ⅱ中正极反应均是O2+2H2O+4e-4OH-
C. 装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动
D. 放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大
科目:高中化学 来源: 题型:
【题目】向饱和食盐水中通入氯化氢,直至有白色固体析出,析出过程中叙述错误的是
A.白色固体是 NaClB.溶液中存在两种电离平衡
C.溶液 pH 值减小D.NaCl 的溶解速率小于结晶速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,能够成立的是( )
CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,能够成立的是( )
A. 其他条件不变仅将容器的体积缩小一半,反应速率减小
B. 反应达平衡状态时:v正(CO)=v逆(H2O)
C. 保持体积不变,充入少量He使体系压强增大,反应速率一定增大
D. 其他条件不变,适当增加C(s)的质量会使反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( ) 
A.反应的化学方程式:N2M
B.t2时,正、逆反应速率相等,达到平衡
C.t2时,正反应速率大于逆反应速率
D.恒温恒容下,当N的化学反应速率是M的两倍时,则证明达到了化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:15P、33As位于同一主族,下列关系正确的是
A. 原子半径:As>Cl>P B. 热稳定性:HCl>PH3>AsH3
C. 非金属性:Cl>As>S D. 酸性:H3AsO4>H2SO4>H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:

请回答下列问题:
(1)当(NH4)2SO4,NH3·H2O的混合溶液中存在c(NH4+)=2c(SO42-)时,溶液呈___________ (填“酸”、“碱”或“中”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是__________________(任写一种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为____________________________。
(4)“沉锌”的离子方程式为__________________________________。
(5)“过滤III”所得滤液可循环使用,其主要成分的化学式是__________________。
(6)己知:HCN的电离常数Ka=4.9×10 -10, H2S 的电离常数Ka1=1.3×10 -7,Ka2=7.0×10 -15,向NaCN 溶液中通入少量的H2S 气体,反应的离子方程式为______________________________________。在废水处理领域中常用H2S 将Mn2+转化为MnS 除去,向含有0.020 molL-1Mn2+废水中通入一定量的H2S 气体,调节溶液的pH=a,当HS-浓度为1.0×10 -4molL-1时,Mn2+开始沉淀,则a=____________。[已知: Ksp(MnS)=1.4×10 -15]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Cl、N、S等非金属元素单质及其化合物的说法正确的是
A. 实验室可用浓硫酸干燥氨气
B. 陶瓷、水晶、水泥、玻璃都属于硅酸盐产品
C. 漂白粉变质后的残留固体有碳酸钙
D. 单质氯气及单质硫与铁反应生成的产物中,铁的化合价相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基态原子的核外电子排布为4d105s1的元素应在( )
A.s区、第五周期、ⅠA族B.ds区、第五周期、ⅠB族
C.d区、第四周期、ⅠB族D.ds区、第五周期、ⅠA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com