
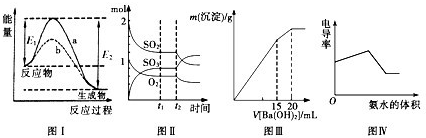
| A.图I表示某放热反应在无催化剂(a)和有催化剂(b)时反应的能量变化 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3各成分的物质的量变化,t2时刻改变的条件可能是增加了SO2 2SO3各成分的物质的量变化,t2时刻改变的条件可能是增加了SO2 |
| C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mLBa(OH)2溶液时铝离子恰好沉淀完全 |
| D.电导率可表示溶液导电性的强弱,电导率越大导电性越强。图Ⅳ可表示向盐酸和醋酸混合溶液中滴入氨水过程中电导率的变化关系 |
 2SO3 达到平衡后依据图Ⅱ分析二氧化硫和氧气物质的量减小,三氧化硫物质的量增大,不可能是增加SO2,错误;C、明矾溶液中加入Ba(OH)2溶液,开始生成BaSO4和Al(OH)3沉淀,中间继续生成BaSO4但Al(OH)3溶解,所以质量增加变慢,最后都是BaSO4沉淀,沉淀质量不再变化,错误;D、向盐酸和醋酸混合溶液中滴入氨水发生反应生成强电解质氯化铵和醋酸铵,溶液的导电性增强,继续滴加氨水,导电能力不会迅速减小,错误。
2SO3 达到平衡后依据图Ⅱ分析二氧化硫和氧气物质的量减小,三氧化硫物质的量增大,不可能是增加SO2,错误;C、明矾溶液中加入Ba(OH)2溶液,开始生成BaSO4和Al(OH)3沉淀,中间继续生成BaSO4但Al(OH)3溶解,所以质量增加变慢,最后都是BaSO4沉淀,沉淀质量不再变化,错误;D、向盐酸和醋酸混合溶液中滴入氨水发生反应生成强电解质氯化铵和醋酸铵,溶液的导电性增强,继续滴加氨水,导电能力不会迅速减小,错误。

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源:不详 题型:单选题
| | KCl | K2SO4 | ZnCl2 | ZnSO4 |
| 甲 | 0.3 mol·L-1 | 0.2 mol·L-1 | 0 | 0.1 mol·L-1 |
| 乙 | 0.1 mol·L-1 | 0.3 mol·L-1 | 0.1 mol·L-1 | 0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.少量的CO2通人氨水中:CO2+NH3·H2O=NH4++HCO3- |
B.Na2O2溶于水中:2Na2O2+2H2O=4Na++4OH-+O2 |
| C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ |
D.用惰性电极电解熔融氯化钠:2C1-+2H2O Cl2 Cl2 +H2 +H2 +2OH- +2OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B.在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| C.在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
| D.在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe2+ | B.Al3+ | C.Fe3+ | D.NH4+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
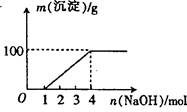
| A.②⑤⑥⑦ | B.②③⑤⑦ |
| C.①②③⑥⑦ | D.①②③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
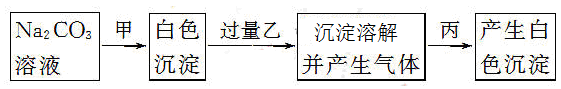
| A.BaCl2、H2SO4、MgCl2 | B.CaCl2、HNO3、BaCl2 |
| C.CaCl2、HNO3、NaCl | D.BaCl2、HCl、Na2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
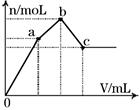
| A.NH4Al(SO4)2 | B.KAl(SO4)2 |
| C.Al2(SO4)3 | D.Na2SO4与NaAlO2组成的混合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 现象和结论 |
| 步骤1:取少量吸收液于试管,滴加稀硫酸酸化,然后再滴入几滴 溶液。 | 现象: 结论:假设1不成立。 |
| 步骤2: | 现象: 结论:假设2成立。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com