
| A、0.21 mol |
| B、0.25 mol |
| C、0.3 mol |
| D、0.35 mol |
| 2.24L |
| 22.4L/mol |
| 0.6mol |
| 2 |


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
| A、丙烷完全燃烧的热化学方程式为C3H8+5O2═3CO2+4H2O△H=-2 036 kJ/mol |
| B、C3H8(g)+5O2(g)═3CO2(g)+4H2O(g);△H<-2 036 kJ/mol |
| C、丙烷完全燃烧的热化学方程式为:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=2 036 kJ/mol |
D、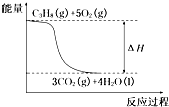 丙烷燃烧的能量变化可用如图所示表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室需要0.5mol?L-1硫酸溶液480ml.根据这两种溶液的配制情况回答下列问题:
实验室需要0.5mol?L-1硫酸溶液480ml.根据这两种溶液的配制情况回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| t/s | 0 | 500 | 1 000 |
| c(H2)/(mol?L-1) | 5.00 | 3.52 | 2.48 |
| c (CO)/(mol?L-1) | 2.50 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16 gCH4与18 gNH4+所含质子数相等 |
| B、CH4O和C2H6O都符合CnH2n+2O的通式,它们可能互为同系物 |
| C、32S与33S的质子数相等,属于同一种元素的不同原子 |
| D、质量相等、体积不等的N2和C2H4的分子数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、a 为电源的负极 | ||||
| B、Fe电极的电极反应是4OH--4e-=2H2O+O2↑ | ||||
| C、通电一段时间后,铁电极附近溶液先变红 | ||||
D、电解饱和食盐水的化学方程式是2NaCl+2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
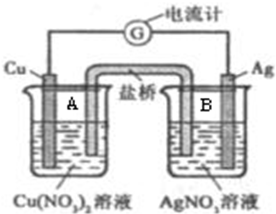 某原电池构造如图所示.其电池的总反应是:Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s).请回答以下问题:
某原电池构造如图所示.其电池的总反应是:Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s).请回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com