
【题目】短周期元素形成的纯净物A、B、C、D、E,五种物质之间的转化关系如图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的一种相同)。

请回答下列问题:
(1)若C是离子化合物,D是一种强碱,则C的化学式________,并任写一种C的主要用途 。
(2)若E的水溶液呈弱酸性,D是既能溶于强酸、又能溶于强碱的化合物。
①用电离方程式解释D既能溶于强酸、又能溶于强碱的原因(仅写出电离方程式即可): ________________________。
②用电荷守恒的等式表示E与NaOH溶液反应生成正盐的溶液中所有离子的浓度之间的关系:________________________________。
(3)若C是一种气体,D是一种强酸,则:
①C与水反应的化学方程式为_____________________________________。
②已知常温下物质A与物质B反应生成1 mol气体C的ΔH=-57 kJ·mol-1,1 mol气体C与H2O反应生成化合物D和气体E的ΔH=-46 kJ·mol-1,写出物质A与物质B及水反应生成化合物D的热化学方程式为__________________________________________。
③有人认为“浓H2SO4可以干燥气体C”。某同学为了验证该观点是否正确,用如图所示装置进行实验。
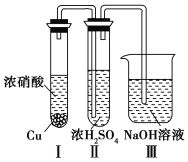
实验过程中,在浓H2SO4中未发现有气体逸出,则得出的结论是____________________________。
④用铂做电极电解H2SO4的溶液,其阳极的电极反应式为 。
【答案】(1)Na2O2 供氧剂、漂白剂、氧化剂均可
(2)①H++H2O+![]()
![]() Al(OH)3
Al(OH)3![]() Al3++3OH-
Al3++3OH-
②c(Na+)+c(H+) =2c(S2-)+c(HS-)+c(OH-)
(3)①3NO2+H2O![]() 2HNO3+NO
2HNO3+NO
②4NO(g)+3O2(g)+2H2O(l) ![]() 4HNO3(aq) ΔH=-618 kJ·mol-1
4HNO3(aq) ΔH=-618 kJ·mol-1
③NO2能溶于浓硫酸中,浓硫酸不能干燥NO2
④2H2O-4e-![]() O2 ↑+4H+
O2 ↑+4H+
【解析】本题考查无机推断,钠的重要化合物的性质,溶液中离子浓度大小的比较,氮的重要化合物的化学性质,热化学方程式的书写,电解原理。
(1)离子化合物与水反应生成气体和碱,C是过氧化钠Na2O2,可以作供氧剂、漂白剂、氧化剂。
(2)若E的水溶液呈弱酸性,D是既能溶于强酸、又能溶于强碱的化合物,化合物C遇水发生双水解,C是硫化铝,水解生成硫化氢气体和氢氧化铝沉淀。
①氢氧化铝是两性氢氧化物,可以按酸式电离Al(OH)3![]() H++H2O+
H++H2O+![]() ,也可以按碱式电离Al(OH)3
,也可以按碱式电离Al(OH)3 ![]() Al3++3OH-。
Al3++3OH-。
②E与NaOH溶液反应生成正盐硫化钠的溶液中所有离子的浓度之间的关系:c(Na+)+c(H+) =2c(S2-)+c(HS-)+c(OH-)
(3)若C是一种气体,D是一种强酸,则:
①C是二氧化氮,与水反应的化学方程式为:3NO2+H2O![]() 2HNO3+NO
2HNO3+NO
②A、B反应生成C的反应方程式为:NO(g)+ ![]() O2
O2![]() NO2(g) ΔH=-57 kJ·mol-1,C与水反应生成D和E的热化学方程式为:NO2(g)+
NO2(g) ΔH=-57 kJ·mol-1,C与水反应生成D和E的热化学方程式为:NO2(g)+![]() H2O(l)
H2O(l) ![]()
![]() HNO3(aq)+
HNO3(aq)+![]() NO(g) ΔH=-46 kJ·mol-1,根据盖斯定律,物质A与物质B及水反应生成化合物D的热化学方程式为:4NO(g)+3O2(g)+2H2O(l)
NO(g) ΔH=-46 kJ·mol-1,根据盖斯定律,物质A与物质B及水反应生成化合物D的热化学方程式为:4NO(g)+3O2(g)+2H2O(l) ![]() 4HNO3(aq) ,ΔH=6(5746)kJ·mol-1=-618 kJ·mol-1
4HNO3(aq) ,ΔH=6(5746)kJ·mol-1=-618 kJ·mol-1
③实验过程中,在浓H2SO4中未发现有气体逸出,说明气体二氧化氮能溶于浓硫酸,浓硫酸不能干燥NO2
④用铂做电极电解H2SO的溶液,其阳极上水放电生成氧气,电极反应式为:2H2O-4e-![]() O2 ↑+4H+。
O2 ↑+4H+。


科目:高中化学 来源: 题型:
【题目】已知OCN-中每种元素都满足8电子稳定结构,在反应OCN-+OH-+C12→CO2+N2+C1-+H2O(未配平)中,如果有6 mol C12完全反应,则被氧化的OCN-的物质的量是
A. 2 mol B. 3 mol C. 4 mol D. 6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)2C(g)达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物的量浓度、反应速率分别随时间的变化如图所示:下列说法中正确的是( )
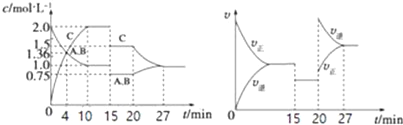
A. 4 min时反应第一次达到平衡
B. 15 min时降低压强,20 min时升高温度
C. 反应方程式中的x=1,正反应为吸热反应
D. 15~20 min该反应使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017江苏]通过以下反应可获得新型能源二甲醚(CH3OCH3 )。下列说法不正确的是
①C(s) + H2O(g)![]() CO(g) + H2 (g) ΔH1 = a kJ·mol1
CO(g) + H2 (g) ΔH1 = a kJ·mol1
②CO(g) + H2O(g)![]() CO2 (g) + H2 (g) ΔH 2 = b kJ·mol1
CO2 (g) + H2 (g) ΔH 2 = b kJ·mol1
③CO2 (g) + 3H2 (g)![]() CH3OH(g) + H2O(g) ΔH 3 = c kJ·mol1
CH3OH(g) + H2O(g) ΔH 3 = c kJ·mol1
④2CH3OH(g)![]() CH3OCH3 (g) + H2O(g) ΔH 4 = d kJ·mol1
CH3OCH3 (g) + H2O(g) ΔH 4 = d kJ·mol1
A.反应①、②为反应③提供原料气
B.反应③也是CO2资源化利用的方法之一
C.反应CH3OH(g)![]()
![]() CH3OCH3 (g) +
CH3OCH3 (g) +![]() H2O(l)的ΔH =
H2O(l)的ΔH =![]() kJ·mol1
kJ·mol1
D.反应 2CO(g) + 4H2 (g)![]() CH3OCH3 (g) + H2O(g)的ΔH = ( 2b + 2c + d ) kJ·mol1
CH3OCH3 (g) + H2O(g)的ΔH = ( 2b + 2c + d ) kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组为了要探究实验室制备 Cl2 的过程中会有水蒸气和 HCl 挥发出来,同时要 证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
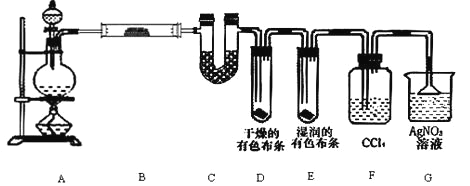
(1)若用含有 0.2mol HCl 的浓盐酸与足量的 MnO2 反应制 Cl2,制得的 Cl2 在标准状况下体积总 是________________1.12L(填“大于”或“等于”或“小于”),原因是________________。
(2)①装置 B 中盛放的试剂名称为__________,作用是________________
②装置 D 和 E 中出现的不同现象说明了________________
③装置 F 的作用是________________
④写出装置 G 中发生主要反应的离子方程式为________________.
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入 AgNO3 溶液中的气体只有一种.为了 确保实验结论的可靠性,证明最终通入 AgNO3 溶液的气体只有一种,乙同学提出在某两个装置之间 再加一个装置.你认为该装置应加在________________与________________之间(填装置字母序号),装置中应放入________________(填写试剂或用品名称).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+ F2(g)===2HF(g)的能量变化如图所示,下列有关叙述中正确的是( )

A. 氟化氢气体分解生成氢气和氟气的反应是放热反应
B. 1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ
C. 在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量
D. 断裂1 mol H—H键和1 mol F—F键吸收的能量大于形成2 mol H—F键放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大力发展电动汽车,可以有效控制空气污染。目前机动车常使用的电池有铅蓄电池、锂电池等。
I.铅蓄电池充放电的总反应为:PbO2+Pb+2H2SO4 ![]() 2PbSO4+2H2O,锂硫电池充放电的总反应为:2Li+S
2PbSO4+2H2O,锂硫电池充放电的总反应为:2Li+S![]() Li2S。
Li2S。
(1)82Pb的原子结构示意图为 。铅蓄电池的正极材料为_________。
(2)当消耗等质量的负极活性物质时,锂硫电池的理论放电量是铅蓄电池的 ____倍。(保留三位有效数字)。
(3)古代用PbSO4作油画的白色颜料,置于空气会慢慢变成黑色的PbS,从而使油画色彩变暗。用H2O2清洗可使油画“复原”。用化学方程式表示该复原的原理________。
II.由方铅矿(PbS)制备铅蓄电池电极材料(PbO2)的方法如下:
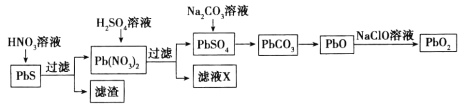
(4)滤液X是一种可循环使用的物质,其溶质主要是__________________(填化学式),若X中残留的![]() 过多,循环使用时可能出现的问题是___________________________。
过多,循环使用时可能出现的问题是___________________________。
(5)向 PbSO4中加Na2CO3溶液会发生:PbSO4 (s)+ ![]() (aq)
(aq)![]() PbCO3 (s)+
PbCO3 (s)+ ![]() (aq)。已知25℃时,Ksp(PbSO4)= 1.8×10-8,Ksp(PbCO3)=1.5×10-13。列式并计算该反应此温度下的平衡常数K 。(提示:需写出K的表达式、代入数据、算出结果)
(aq)。已知25℃时,Ksp(PbSO4)= 1.8×10-8,Ksp(PbCO3)=1.5×10-13。列式并计算该反应此温度下的平衡常数K 。(提示:需写出K的表达式、代入数据、算出结果)
(6)以石墨为电极电解Pb(NO3)2溶液也可以制得PbO2。PbO2将在 极生成(填“阴”或“阳”);而另一极的电极反应式为 ,故Pb元素的利用率较低。若在Pb(NO3)2溶液中加入适量Cu(NO3)2则可有效利用Pb2+,其理由是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素-4是一种激光染料,应用于可调谐染料激光器。香豆素-4由C、H、O三种元素组成,分子球棍模型如图所示。下列有关叙述正确的是

①分子式为![]()
②能与饱和溴水发生取代反应
③能与饱和溴水发生加成反应
④能使酸性![]() 溶液褪色
溶液褪色
⑤1mol香豆素-4最多能与含1molNaOH的溶液反应
A. ①②③ B. ③④⑤ C. ②③④ D. ②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com