
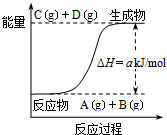
| A. | 该体系的压强不变时标志此反应处于平衡状态 | |
| B. | 若该反应中有电子得失,则可设计成原电池 | |
| C. | 反应物的总键能高于生成物的总键能 | |
| D. | 该反应中的反应物A和B的转化率一定相同 |
分析 A.A+B?C+D反应中ABCD都是气体,反应前后压强始终不变;
B.若该反应中有电子得失为氧化还原反应,反应是吸热反应,不一定能自发进行;
C.反应焓变=反应物的总键能-生成物的总键能;
D.转化率等于消耗量除以起始量,若起始量不同,消耗量相同,转化率不同.
解答 解:A.图象分析可知,反应无能量低于生成物,反应为吸热反应,A+B?C+D反应中ABCD都是气体,反应前后压强始终不变,压强不变不能说明反应达到平衡状态,故A错误;
B.若该反应中有电子得失为氧化还原反应,反应是吸热反应,不一定能自发进行,非自发进行的氧化还原反应不能设计为原电池,故B错误;
C.当反应物的总键能高于生成物的总键能反应的焓变为正值,反应为吸热反应,符合图象变化,故C正确;
D.反应物A和B的转化率和起始量变化量有关,若起始量不同,转化率也不同,故D错误;
故选C.
点评 本题考查了化学反应能量变化分析,图象分析方法和应用,注意反应吸热放热和反应条件关系的判断应用,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 阴离子的还原性:Z>Y>X | B. | 单质的非金属性:X>Y>Z | ||
| C. | 气态氢化物的稳定性:X<Y<Z | D. | 原子原子半径:X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时向水中加入少量固体CH3COONa,平衡逆向移动,c (H+)降低,Kw不变 | |
| B. | 由水电离出的c(H+)=10-12mol•L-1的溶液中:Na+、Ba2+、HCO3-、Cl-可以大量共存 | |
| C. | 向Na2CO3溶液中加入NaOH溶液后,c(CO32- )减少 | |
| D. | 某温度时的混合溶液中c(H+)=$\sqrt{{K}_{W}}$mol•L-1,说明该溶液呈中性(KW为该温度时水的离子积常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H++2e-=H2↑ | B. | Fe=Fe2++2e- | ||
| C. | 2H2O+O2+4e-=4OH- | D. | 4OH-=2H2O+O2↑+4e- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com