
某学习小组对原电池的构成及形成条件做如下探究性实验,请你推测可能的现象,并给出合理的解释。
| 编号 | 装置图示 | 实验内容 | 现象 | 解释或说明 |
| 1 |
| Cu、Zn同时插入,但不接触 | ||
| 2 | 将Cu、Zn用导线连接起来并接电流计 | |||
| 3 |
| Zn、Zn与稀硫酸进行实验 | ||
| 4 | Cu、石墨与稀硫酸进行实验 | |||
| 5 | Zn、石墨与稀硫酸进行实验 |
科目:高中化学 来源: 题型:
根据表中信息判断,下列选项不正确的是
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO | Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO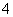 >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
中学常见反应的化学方程式有A+B→X+Y+H2O或H2O+ A+B→X+
Y(未配平,反应条件略去),下列问题所涉及反应式中的H2O已经略去。请回答:
(1)常温下,若A为黄绿色气体,B为非金属氧化物,A、B均能使品红溶液褪色,A+B→X+Y,且相对分子质量X>Y,则该反应的化学方程式为________________,检验Y中阴离子的试剂是________________。
(2)若Y是黄绿色气体,且A、B的物质的量之比为1∶4,该反应的化学方程式是 。
(3)若A为常见的金属单质,Y为气态单质,B溶液呈强酸性或强碱性时,A和B反应都能进行。写出A与B反应的离子方程式:_________________;_________________。
(4)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,其中A、B的物质的量之比为1∶4,则反应中氧化剂与还原剂的物质的量之比是 。
(5)若A、B均为化合物,Y为白色沉淀(不含金属元素),B为引起温室效应的主要气体,将B通入某溶液后可生成Y,写出Y可能的化学式______________。写出生成Y的一个离子方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于能量转化的认识不正确的是( )
A.绿色植物的光合作用是将光能转变为化学能
B.煤燃烧时化学能转变成热能和光能
C.原电池工作时,化学能转变为电能
D.白炽灯工作时,电能全部转变成光能
查看答案和解析>>
科目:高中化学 来源: 题型:
根据反应:2Ag++Cu===Cu2++2Ag,设计如图所示原电池,下列说法错误的是( )
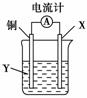
A.X可以是银或石墨
B.Y是硫酸铜溶液
C.电子从铜电极经外电路流向X电极
D.铜极上的电极反应式为:Cu-2e-===Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)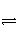
 2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( )
①C生成的速率与C分解的速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④A、B、C的压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
A.②⑧ B.①⑥ C.②④ D.③⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g) 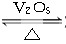 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=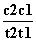
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。如图所示为它们的结构简式。下列关于这两种有机化合物的说法中正确的是( )
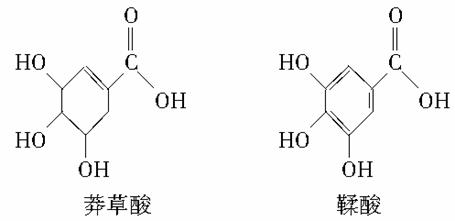
A.两种酸都能与溴水反应
B.两种酸遇三氯化铁溶液都显色
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.等物质的量的两种酸与足量金属钠反应产生氢气的量不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com