
���ĸ������ǩ���Լ�ƿ�У��ֱ�ʢ�����ᡢBaCl2��Һ��Na2CO3��Һ��AgNO3��Һ��Ϊ�˼����ƿ�е��Լ������Ƿֱ���ΪA��B��C��D��������ϣ���ʵ������Ϊ��A��B������ɫ���壻B��C������ɫ������A��D������ɫ������A��C�����Ա仯��
��1���ɴ��Ƴ����Լ�ƿ��ʢ���Լ�Ϊ(�ѧʽ)��
A��________��B��________��C________��D________��
��2��A��B��Ӧ�����ӷ���ʽΪ______________________________��
��3��A��D��Ӧ�����ӷ���ʽΪ______________________��
 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��Ӧ��2SO2��g��+O2��g��⇌2SO3��g����H��0��ij�¶��£���2mol SO2��1mol O2����10L�ܱ������У���Ӧ��ƽ���SO2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ����ʾ��������˵����ȷ���ǣ�������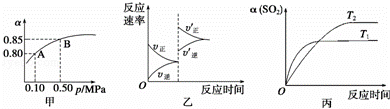
| �� | A�� | ��ͼ��֪��A��SO2��ƽ��Ũ��Ϊ0.4 mol/L |
| �� | B�� | ��ͼ��֪��B��SO2��O2��SO3��ƽ��Ũ��֮��Ϊ2��1��2 |
| �� | C�� | ��ƽ�����С�����ݻ�����Ӧ���ʱ仯ͼ�������ͼ�ұ�ʾ |
| �� | D�� | ѹǿΪ0.50 MPaʱ��ͬ�¶���SO2ת�������¶ȹ�ϵ���ͼ����T2��T1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������λ�ڶ����ڵ��������ڡ���������ķǽ���Ԫ��X��Y����֪��Ԫ������������ˮ�����Ϊǿ�ᣮ������ͼת����ϵ����Ӧ���������ֲ�������ȥ�����ش��������⣺
��1����A��B��C��D��Ϊ��XԪ�صĻ������A��F��һ�������ж�ֻ����10�����ӣ���
��A���ӵĿռ乹��Ϊ�������Ρ���F���ӵĵ���ʽΪ��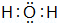 ����
����
�ڷ�Ӧ I �Ļ�ѧ����ʽΪ��4NH3+5O2 4NO+6H2O����
4NO+6H2O����
�ۻ�����NaX3�Ǻϳɡ���ơ����м�������ʣ�Ҳ��������ȫ�����е���Ҫ���ʣ�NaX3��ײ��������Na3X����һ�����嵥�ʣ���д���÷�Ӧ�Ļ�ѧ����ʽ��3NaN3=Na3N+4N2������
��X�����������γɹ⻯ѧ����ԭ��֮һ����ҵ�Ͽɲ����������⻯�ﷴӦ�����������ʶ���ȥ�����÷���ʽ��ʾ�÷�Ӧ��6NOx+4xNH3=��3+2x��N2+6xH2O����
��2����A��B��C��D��Ϊ��YԪ�صĻ��������A������Ԫ����ɣ���A��Ħ������Ϊ120g•mol��1����
�ٽ���ӦIV���õ���Һ�������ɵõ��ľ������ڡ����ӡ����壨����ӡ��������ӡ�����ԭ�ӡ���
�ڷ�Ӧ I �Ļ�ѧ����ʽΪ��4FeS2+11O2 2Fe2O3+8SO2����
2Fe2O3+8SO2����
�ۺ�YԪ�صĻ�����Na2Y�ʹ���������Һ��ǿ���Ի������ܷ�����Ӧ��������������д���÷�Ӧ�����ӷ�Ӧ����ʽ��S2��+4ClO��=SO42��+4Cl������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ��һ���ܴ���������� (����)
A��0.1 mol·L��1 NaOH��Һ��K����Na����SO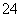 ��CO
��CO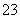
B��0.1 mol·L��1 Na2CO3��Һ��K����Ba2����NO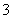 ��Cl��
��Cl��
C��0.1 mol·L��1 FeCl3��Һ��K����NH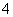 ��I����SCN��
��I����SCN��
D��c(H��)/c(OH��)��1��1014����Һ��Ca2����Na����ClO����NO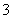
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��д��ȷ���� (����)
A����ˮ��ͨ��������Cl2��H2O 2H����Cl����ClO��
2H����Cl����ClO��
B�����Ȼ�����Һ�м���ͭ��2Fe3����3Cu===2Fe��3Cu2��
C��NH4HCO3��Һ�����KOHŨ��Һ���ȣ�NH ��OH��
��OH�� NH3����H2O
NH3����H2O
D������������еμ�Ũ���Ტ���ȣ�MnO2��4H����2Cl�� Mn2����Cl2����2H2O
Mn2����Cl2����2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±��ж����ӷ���ʽ�����۲���������
| ѡ�� | ��ѧ��Ӧ�����ӷ���ʽ | ���� |
| A | NaClO��Һ��ͨ��������SO2��ClO����H2O��SO2===Cl����SO | �����Խ����в���������H�� |
| B | �����Ը��������Һ�ζ����2MnO | ��ȷ |
| C | NH4Al(SO4)2��Һ�е��뼸��NaOH��Һ��NH | ����OH�����Ⱥ�Al3����Ӧ����Al(OH)3���� |
| D | �ö��Ե缫���MgCl2��Һ��2Mg2����2H2O | ��ȷ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B��C��D�������ʾ�Ϊ����������ɵĿ����Ի����������������ʵ����ӣ����Ӳ����ظ���ϣ��У�
| ������ | Na+��Al3+��Ba2+��NH4+ |
| ������ | Cl |
�ֱ�ȡ�������ʽ���ʵ�飬ʵ�������¢�B��Һ�ֱ���C��D��ϣ����а�ɫ�������ɢڽ�A��Һ��ε���C��Һ�У��г������ɣ������μ�A��Һʱ����������ֱ����ȫ��ʧ��A��D���ֹ��������������ɣ���������ʹʪ��ĺ�ɫʯ����Һ��������ʯī�缫���B��Һ���������ϲ���һ���д̼�����ζ������
�ش��������⣺
��1��A�����������Ӻ�C���������ӵİ뾶��С_��___��___��___�������ӷ��ţ���B��������������____��____
��2��C��Һ��__��_�ԣ�����ԡ����ԡ�������ԭ����______��____________
�������ӷ���ʽ���ͣ���D�Ļ�ѧʽ��_____��_______
��3����PtΪ�缫���1L0.1mol/LB��ˮ��Һ������·��ͨ��0.1mol����ʱ��
��Һ��pHΪ___��____�����������Һ������䣩�������ĵ缫��ӦʽΪ��___��__
��4����������������������ͨ��A��Һ����ǡ����ȫ��Ӧʱ������Һ�и�����
Ũ���ɴ�С������˳��Ϊ____________��______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±��ж�Ӧ��ϵ��ȷ����
| A | CH3CH3+Cl2 CH2=CH2+HCl | ��Ϊȡ |
| B | ����֬�õ����� �ɵ��۵õ������� | ��������ˮ�ⷴӦ |
| C | Cl2+2Br‾=2Cl‾+Br2 Zn+Cu2+=Zn2++Cu | ��Ϊ���ʱ���ԭ���û���Ӧ |
| D | 2Na2O2+2H2O+4NaOH+O2�� Cl2+H2O=HCl+HClO | ��Ϊˮ����ԭ����������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������������м�����Ҫ�����ã��������й��ס���Ч���Ͷ���ɱ�������������ǽ��չ�����ơ�
��1��Cl2��H2O2��ClO2(��ԭ����ΪCl��)��O3(1 mol O3ת��Ϊ1 mol O2��1 mol H2O)�����ʳ��������������������ʵ�����������������Ч����ߵ���________(�����)��
A��Cl2 B��H2O2 C��ClO2 D��O3
��2��H2O2��ʱ����Ϊ��ҵ��Һ���������С���ɫ�������������ơ��������ɿ�ҵ��Һ�е��軯��(��KCN)�������·�Ӧʵ�֣�KCN��H2O��H2O2===A��NH3������������A�Ļ�ѧʽΪ________��H2O2����Ϊ����ɫ����������������_________________��
��3��Ư����������(NaClO2)�ڳ�����ڰ����ɱ���һ�ꡣ������ȶ��ɷֽ⣬��Ӧ�����ӷ���ʽΪHClO2����ClO2����H����Cl����H2O(δ��ƽ)���ڸ÷�Ӧ�У�����1 mol ClO2����ʱת�Ƶĵ��Ӹ���ԼΪ____________��
��4����84������Һ(��Ҫ�ɷ���NaClO)�ͽ��(��Ҫ�ɷ���Ũ����)���ܻ��ã�ԭ����__________________________________(�����ӷ���ʽ��ʾ)�������ȼ ҵ�IJ������������84������Һ��д���йط�Ӧ�Ļ�ѧ����ʽ��______________________________��
ҵ�IJ������������84������Һ��д���йط�Ӧ�Ļ�ѧ����ʽ��______________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com