
食盐中含有一定量的杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的。
已知:①氧化性:IO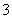 >Fe3+>I2;②KI+I2KI3
>Fe3+>I2;②KI+I2KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Fe2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为四份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①向第四份试液中加K3Fe(CN)6溶液,根据是否得到具有特征蓝色沉淀的盐,可检验溶液中是否含有Fe2+,推测该蓝色沉淀是_______
(用化学式表示)。
②第二份试液中加入足量KI固体后,反应的离子方程式为:____________________、____________________。
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失写出潮湿环境下KI与氧气反应的化学方程式:____________________。
将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质不适合作为食盐加碘剂,其理由是________________________。
科目:高中化学 来源: 题型:
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液体积是
A.60 mL B.45 mL C.30 mL D.15 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关的离子方程式或化学方程式中正确的是( )
A.向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++HCO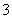 +OH-===CaCO3↓+H2O
+OH-===CaCO3↓+H2O
B.磷酸一氢钠溶液水解:HPO +H2OPO
+H2OPO +H3O+
+H3O+
C.将2 mol SO3气体通入一密闭容器中,达平衡后吸收Q kJ热量,则该反应的热化学方程式为2SO3(g)2SO2(g)+O2(g) ΔH=+Q kJ/mol
D.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2,充分反应:4Fe2++2Br-+3Cl2===4Fe3++6Cl-+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组微粒在指定的溶液中一定能大量共存的是( )
A.加入金属镁产生H2的溶液中:NH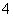 、Na+、SO
、Na+、SO 、CH3COO-
、CH3COO-
B.含有大量ClO-的溶液中:K+、Na+、NO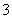 、SO
、SO
C.c(Cu2+)=0.1 mol·L-1的溶液中:H+、NH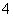 、Br-、CO
、Br-、CO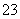
D.含有大量MnO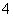 的溶液中:H+、SO
的溶液中:H+、SO 、Cl-、CH3CH2OH
、Cl-、CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气,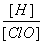 减小
减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有[Na+]=[Cl-]+[ClO-]
D.加入少量水,水的电离平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
在盛有溴水的三支试管中分别加入少量苯、四氯化碳和酒精,振荡后静置,出现下列现象,正确的结论是 ( )

A.①加CCl4 ②加苯 ③加酒精
B.①加酒精 ②加CCl4 ③加苯
C.①加苯 ②加CCl4 ③加酒精
D.①加苯 ②加酒精 ③加CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组利用MnO2和浓HCl及如图装置制备Cl2。下列分析中不正确的是( )

A.A中可用分液漏斗代替长颈漏斗
B.A中缺少加热装置
C.B中盛放的NaOH溶液可以净化C l2
l2
D.D中的导管口若连接倒置漏斗可防止倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是
A.产生气体的体积:①>②
B.①的溶液复原可向电解后的溶液中加氯化铜;②中电解后溶液的pH不变
C.电极上析出物质的质量:①>②
D.电极反应式:①中阳极2Cl- -2e- = Cl2↑②中负极 2H+ + 2e- = H2↑

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com