
����Ŀ�������������ĺ��������Ϊ��ɫ��״���壬�����ڱ�ͪ���ȷºͱ��У��ڼ״����Ҵ������ѡ�ʯ�����п��ܽ⣬��ˮ�м������ܣ��۵�Ϊ156��157�������ȶ��Բ�������Ǹ�Ч�Ŀ�űҩ����֪�����ѷе�Ϊ35��������������ȡ�����صķ���֮һ������ȡԭ��Ϊ�����ģ���Ҫ�����ѽ�ȡ�������ͽ�ȡ�������ѽ�ȡ������Ҫ����Ϊ��

��ش��������⣺
��1����������и��������Ŀ����__________��
��2����������Ҫ�IJ���������Ҫ�У��ձ�����������__________����������������__________����������������__________��
��3��ͨ����ȼ�յķ����ⶨ�л���ķ���ʽ������ȼ�����ڽ��л�����Ʒ�봿���ڵ�¯�����³��ȼ�գ����ݲ�Ʒ������ȷ���л������ɡ���ͼ��ʾ������ȼ�շ�ȷ�������ط���ʽ��װ�á�

�������������IJ�����Ϣ��װ�õ�����˳��Ӧ��__________��ÿ��װ������һ������
����ʵ��װ�ÿ��ܻ��������ɲⶨ������ƫ�ͣ��Ľ�������__________��
����������Ʒ������Ϊ28.2 g���ú����Ľ����װ�������������Ƶ�A������66 g��B������19.8 g������������������ʽ��__________��
��Ҫȷ�����л���ķ���ʽ��������֪����������__________��
��4��ijѧ���������ص����ʽ���̽�����������ؼ��뺬��NaOH����̪��ˮ��Һ�У������ص��ܽ�����С�����Ȳ����裬�����ص��ܽ�����������Һ��ɫ��dz���������ػ�ѧ�������Ƶ�������__________������ĸ������
A���Ҵ� B������ C�������� D����������
���𰸡�
��1���������������ѵĽӴ��������������صĽ�ȡ�ʣ�
��2��©���������ؽᾧ��
��3����DCEBA��
����װ��A���һ����ֹ�����е�CO2��ˮ��������A��װ�ã�
��C15H22O5���������ص���Է���������
��4��D��
��������
�����������1����������и�����������������������ѵĽӴ��������������صĽ�ȡ�ʣ��ʴ�Ϊ���������������ѵĽӴ��������������صĽ�ȡ�ʣ�
��2���������ǹ��ˣ���Ҫ�IJ���������Ҫ�У��ձ�����������©�����������������������ؽᾧ���ʴ�Ϊ��©���������ؽᾧ��
��3����ͨ��˫��ˮ�ķֽ���ȡ��������Ũ������������л��ﷴӦ�����ɵ�ˮ����ˮ�Ȼ������գ����ɵĶ�����̼�ü�ʯ�����գ���װ�õ�����˳��ΪDCEBA���ʴ�Ϊ��DCEBA��
��װ�������ļ�ʯ���ܹ����տ����еĶ�����̼��ˮ�������Ľ�����Ϊ����װ��A���һ����ֹ�����е�CO2��ˮ��������A��װ�ã��ʴ�Ϊ����װ��A���һ����ֹ�����е�CO2��ˮ��������A��װ�ã�
�������ݿ�֪ m��H2O��=19.8g������n��H2O��=1.1mol��m��CO2��=66g������ n��CO2��=1.5mol����������������ԭ�ӵ�����Ϊm��O��=28.2-��2.2��1��-��1.5��12��=6g������n��O��=0.5mol��N��C����N��H����N��o��=1.5��2.2��0.5=15��22��5������C15H22O5���ʴ�Ϊ��C15H22O5��
��Ҫȷ�����л���ķ���ʽ��������֪�������ص���Է����������ʴ�Ϊ�������ص���Է���������
��4��������������ˮ����������������Һ��ˮ�Ⲣ�����������ƽ�������֪���������к�����������ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����ܱ������������淴ӦZ��?��+W��?��![]() X��g��+Y��?����H����t1ʱ�̷�Ӧ�ﵽƽ�⣬��t2ʱ����С���������t3ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ����
X��g��+Y��?����H����t1ʱ�̷�Ӧ�ﵽƽ�⣬��t2ʱ����С���������t3ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ����
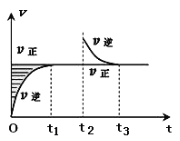
A��Z��W�ڸ�������������һ����Ϊ��̬
B��t1��t2ʱ�����t3ʱ�̺���ʱ��η�Ӧ��ϵ�������ƽ��Ħ���������������
C�����÷�Ӧֻ��ij�¶�T0�����Է����У���÷�Ӧ��ƽ�ⳣ��K���¶����߶�����
D�����ڸ��¶��´˷�Ӧƽ�ⳣ������ʽΪK��c��X������t1��t2ʱ�����t3ʱ�̺��XŨ�Ȳ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵���У���ȷ���ǣ� ��
A. ������ʹKMnO4��Һ��ɫ����˱����ܷ���������Ӧ
B. ��֬���Ҵ�����������Ӫ������
C. �����������������ʹNaOH�ķ�̪��Һ��ɫ����Ϊ���ǵķ�����ɺͽṹ��ͬ
D. �ñ���Na2CO3��Һ���Գ�ȥ���������л��е�����������Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ľ̿��ԭ����ͭ��ʵ���з�������Ҫ��Ӧ��C+2CuO![]() 2Cu+CO2����ij��ѧʵ��С��Ը�ʵ
2Cu+CO2����ij��ѧʵ��С��Ը�ʵ
������������ȫ��Ӧ������������̽����
̽��һ���������ijɷ�
��������⡿ʵ������ǰ���ɫ���壬���ѹ۲쵽�Ϻ�ɫ���壬��ô�ð���ɫ����������ʲô��
���������ϡ�������ͭ��Cu2O��Ϊ��ɫ���壬���Ժ����ᷴӦ��Cu2O+H2SO4�TCuSO4+Cu+H2O��
��������衿����ɫ�����ͭ����ܺ���Cu2O��
�����ʵ�顿ȡ��������ɫ���壬����ϡ���ᣬ����۲쵽_______________��˵��������ȷ��
̽�������ⶨ������Cu2O�ĺ���

���������ϡ�������Ũ����������»�ֽ�ΪCO��CO2
�����ʵ�顿��ȡ������Ʒ6.0g����������ͼװ��D�н���ʵ�飨�̶�װ����ȥ����ʯ��Ϊ�����ƺ��������ƵĻ�����ͨ���ⶨ��Ӧǰ��װ��E�������ﵽʵ��Ŀ�ġ�
��1��֤������ķֽ��������CO2���ڵ���_______________��
��2��װ��C��������__________________��
��3��д��װ��D�з�Ӧ�Ļ�ѧ����ʽ___________________________��
��4������Ϊ����װ��ǰ���漰�IJ��ֲ�������ȷ��˳����_________������ţ���
�ټ��װ�õ������� �ڹر�K2����K1��ʹװ��A�еķ�Ӧ�Ƚ���һ��ʱ��
���������� �ܹر�K1����K2
��5����װ��E�ڷ�Ӧǰ��������ֱ�Ϊ30.1g��31.2g����ù�����Ʒ��Cu2O����������Ϊ__________��
ָ����װ�õIJ���֮����˵����������ɲ�窳��Ľ�����__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�߾���ĵ���A��C11H12O2���ɷ������±仯��
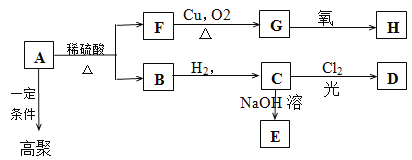
��֪�� C���������ֱ�ȡ�����ɵ�һ�ȴ���D�����֣�F�ķ���ʽΪC7H8O�����б���������FeCl3��Һ����ɫ����ش�
��1��F�����к��еĹ����Žṹ��ʽ�� ��
��2����A����B��F�ķ�Ӧ����Ϊ��ѡ������� ��
��������Ӧ ��ȡ����Ӧ ��ˮ�ⷴӦ ����ȥ��Ӧ
��3��B�Ľṹ��ʽ�� ��
��4������ʽΪC7H8O�����б�����ͬ���칹���F��� �֡�
��5��д�����з���ʽ
�� ��A����B��F�� ��
�� B �� C�� ��
��A��һ�����������ɸ߾�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ж�A(g)��B(g) ![]() C(g)��D(g)�Ƿ�ﵽƽ�������Ϊ(����)
C(g)��D(g)�Ƿ�ﵽƽ�������Ϊ(����)
A. ѹǿ����ʱ��ı�
B. ������ܶȲ���ʱ��ı�
C. c(A)����ʱ��ı�
D. ��λʱ��������C��D�����ʵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƚ�����ȷ����
A. ��̬�⻯���ȶ���HF��HCl��HBr��HI
B. �۵�Rb>K>Na>Li
C. ����RbOH>KOH>NaOH>LiOH
D. ��ԭ��Na��Mg��Al
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�������仯�����ڹ�ũҵ������������������Ҫ�����á���ش��������⣺
��1����CH4 ����ԭNOx �������������������Ⱦ�����磺
��CH4(g)+4NO2(g)=4NO(g)��CO2(g)+2H2O(g) ��H1����574 kJ��mol��1
��CH4(g)+4NO(g)=2N2(g)��CO2(g)+2H2O(g) ��H2
ͬһ�����£���2molCH4 ��ԭNO2 ��N2��������̬ˮ�Ͷ�����̼�����������зų�������Ϊ1734kJ������H2��__________��
��2���ݱ�������ѧ����һ������������Fe2O3����鷴Ӧ����ȡ���������Ľ��������䷴ӦΪ��Fe2O3(s)+3CH4(g)![]() 2Fe(s)+3CO(g)+6H2(g) ��H>0��
2Fe(s)+3CO(g)+6H2(g) ��H>0��
������Ӧ��5L���ܱ������н��У�1min��ﵽƽ�⣬���Fe2O3�ڷ�Ӧ����������3.2g����ö�ʱ����CO��ƽ����Ӧ����Ϊ_______��
�����÷�Ӧ�ں��º�ѹ�����н��У��ܱ����÷�Ӧ�ﵽƽ��״̬����_____������ţ���
A��CH4��ת���ʵ���CO�IJ���
B�����������ܶȱ��ֲ���
C�����ʣ�2v��CO��=v��H2��
D����������������ֲ���
���÷�Ӧ�ﵽƽ��ʱij���������¶ȱ仯��ͼ��ʾ����ѹǿ��P1���ߵ�P2ʱ��ƽ�ⳣ��KA___KB������>������<������=��������������Ա�ʾ������������Щ______��(�����)

A��H2���淴Ӧ����
B��CH4�ĵ�ת����
C����������ƽ����Է�������
D��CO���������
��3��������������ˮ��һԪ���ᡣ
�ٳ����£���1L 0.1mol/L HCOOH��Һ��1L0.1mol/LNaOH��Һ��Ϻ����й�ϵ����ȷ����____������ţ���
a.c(H+)ˮ��c(OH-)ˮ=1��10-14 b.2c(H+)+c(HCOOH)=2c(OH-)+c(HCOO-)
c.c(Na+)=c(HCOOH)+c(HCOO-) d.c(HCOO-)>c(Na+)>c(H+)>c(OH-)
����1L 0.1mol/L HCOONa��Һ�м�ˮϡ�ͺ�c(HCOOH)/c(HCOO-)����ֵ______���������С�����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ�ѧ������ʵ�������������е�Ӧ��������ȷ������������
A. ������ͨ����FeCl2��Һ����ʴͭ��·��
B. ������Na2SiO3��Ϳ������Ч��ֹ���ֵķ���
C. �������Ǻ���ɫ���壬���Խ�������������ɫ�̻�
D. DZˮͧ��һ������������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com