
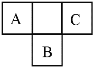
【题目】如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数。B原子核内质子数和中子数相等。下列叙述不正确的是( )
A. C元素是非金属性最强的元素
B. A元素最高价氧化物对应的水化物具有强氧化性
C. B元素的氧化物、氢化物的水溶液都呈酸性
D. 三种元素的原子半径的大小顺序是:B>C>A
【答案】D
【解析】
这几种元素都是短周期元素,A和C属于第二周期元素、B属于第三周期元素,设B原子序数是x,则A的原子序数是x-9、C原子序数是x-7,A、B、C三种元素原子核外电子数之和等于B原子的质量数,B原子核内质子数和中子数相等,则x-9+x+x-7=2x,x=16,所以B是S元素,则A是N元素、C是F元素,据此答题。
A.在周期表中非金属性最强的元素位于周期表右上角(稀有气体除外),所以非金属性最强的元素是F元素,故A正确;
B.氮元素的最高价氧化物的水化物是硝酸,硝酸具有强氧化性,能氧化较不活泼的金属、非金属,如C、Cu等,故B正确;
C.B元素氧化物的水化物有H2SO3、H2SO4,氢化物是H2S,这三种物质都是二元酸,其水溶液都呈酸性,故C正确;
D.B原子电子层数大于A、C,A和C电子层数相等,且A原子序数小于C,所以原子半径大小顺序是B>A>C,故D错误。
故选D。


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A. 铝片与稀H2SO4反应 B. Ba(OH)2·8H2O与NH4Cl反应
C. 灼热的炭与CO2反应 D. 甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)书写下列物质电子式
①Cl2:______________;②CO2:_____________;③H2O2:________________;
(2)用电子式表示下列物质的形成过程
①MgCl2:___________________________;
②H2O:_____________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成![]() 。
。
(1)请写出金属钒与浓硝酸反应的离子方程式:________________________
(2)灼烧![]() 时可生成钒的氧化物
时可生成钒的氧化物![]() 请写出该反应的化学方程式:_________
请写出该反应的化学方程式:_________
(3)![]() 是较强的氧化剂。它能与沸腾的浓盐酸作用产生氯气,其中钒元素被还原为蓝色的
是较强的氧化剂。它能与沸腾的浓盐酸作用产生氯气,其中钒元素被还原为蓝色的![]() 请写出该反应的离子方程式:________________________
请写出该反应的离子方程式:________________________
(4)![]() 是两性氧化物,与强碱反应生成钒酸盐(阴离子为
是两性氧化物,与强碱反应生成钒酸盐(阴离子为![]() ),溶于强酸生成含钒氧离子
),溶于强酸生成含钒氧离子![]() 的盐。请写出
的盐。请写出![]() 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
______________________
(5)工业上用接触法制硫酸时要用到![]() 。在氧化
。在氧化![]() 的过程中,450℃时发生
的过程中,450℃时发生![]() 与
与![]() 之间的转化:
之间的转化:![]() 说明
说明![]() 在接触法制硫酸过程中所起的作用是________________________
在接触法制硫酸过程中所起的作用是________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素X、Y、Z、M、N,其原子半径与原子序数的关系如图,下列说法错误的是( )

A. 非金属性:X>Z
B. 气态氢化物的稳定性:M<N
C. X和Y形成的化合物只可能含离子键
D. M最高价氧化物对应的水化物是一种弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,0.1mol/L的Na2CO3溶液中,下列粒子浓度关系式不正确的是
A. c(Na+)= 2[c(CO32-)+ c(HCO3-)+ c(H2CO3)]
B. c(Na+)+ c(H+)= 2c(CO32-)+ c(HCO3-)+ c(OH—)
C. c(H+)= c(OH-)—c(HCO3-)—c(H2CO3)
D. c(Na+)>c(CO32-)> c(OH—)> c(HCO3-)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于元素周期表和元素周期律的应用有如下叙述:其中正确的是( )
①元素周期表是同学们学习化学知识的一种重要工具;
②利用元素周期表可以预测新元素的原子结构和性质;
③利用元素周期表和元素周期律可以预言新元素;
④利用元素周期表可以指导寻找某些特殊的材料。
A. ①②③④ B. ②③④ C. ③④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(13分)用辉铜矿(主要成分为 Cu2S,含少量Fe2O3、SiO2,等杂质)制备难溶于水的碱式碳酸铜的流程如下:

(1)下列措施是为了加快浸取速率,其中无法达到目的的是____(填字母)。
A.延长浸取时间 | B.将辉铜矿粉碎 |
C.充分搅拌 | D.适当增加硫酸浓度 |
(2)滤渣I巾的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是___________。
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A可以是_______(填化学式);“赶氨”时,最适宜的操作方法是________。
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为_______。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别加到HF溶液、CH3COOH溶液中,两混合溶液中离子浓度与pH的变化关系如图所示,已知pKa=-lgKa,下列有关叙述错误的是

A. 常温下,Ka(CH3COOH)=10-5
B. a点时,c(F-)=c(HF)>c(Na+)>c(H+)>c(OH-)
C. 常温下,0.1mo/LNaF溶液的pH小于0.1mo/LCH3COONa溶液的pH
D. 向CH3COOH溶液中加入NaOH溶液后所得的混合溶液中,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com