
镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有____________________________________________。
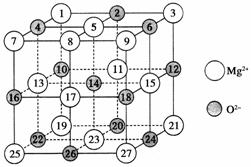
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如上图所示,请改正图中错误:________________。
(3)Mg是第3周期元素,该周期部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1 266 | 1 534 | 183 |
解释表中氟化物熔点差异的原因:________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
科目:高中化学 来源: 题型:
水的沸点是100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是( )
A.范德华力 B.共价键
C.氢键 D.相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.含有金属元素的晶体都是金属晶体
B.金属晶体中不一定含有金属元素
C.具有导电性的晶体一定是金属晶体
D.可以导电的物质形成的晶体不一定是金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
一种金属晶体与一种离子晶体相比较,正确的是( )
A.金属晶体一定比离子晶体微粒堆积得更密集
B.金属晶体一定比离子晶体硬度大
C.金属晶体固态时一定能导电,但离子晶体不能
D.金属晶体一定比离子晶体熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
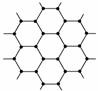
石墨晶体是层状结构(如右图),在每一层内,每一个碳原子都跟其他3个碳原子相结合,据图分析,石墨晶体中碳原子数和共价键数之比为( )
A.2∶3 B.2∶1
C.1∶3 D.3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属的叙述中,不正确的是( )
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键无饱和性和方向性
D.构成金属的自由电子在整个金属内部的三维空间中做自由运动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于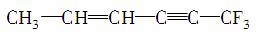 分子结构的叙述中,正确的是( )
分子结构的叙述中,正确的是( )
①6个碳原子可能都在一条直线上 ②6个碳原子不可能都在同一条直线上 ③6个碳原子可能都在同一平面上 ④6个碳原子不可能都在同一平面上
A.①③ B.②③
C.①④ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com