
| A. | ①② | B. | ③⑤ | C. | ④⑥ | D. | ②④ |
分析 根据弱电解质的电离是不完全的,酸的溶解性及酸的通性无法确定酸电离的程度,而比较酸的浓度与酸电离c(H+)可判断酸的电离程度,据此即可解答.
解答 解:①酸溶液都能使紫色石蕊试液变红,1mol/L的HF水溶液能使紫色石蕊试液变红说明HF水溶液显酸性,不能说明HF是弱酸,故①错误;
②HF水溶液中存在HF分子,说明HF在溶液中部分电离,所以能说明HF是弱酸,故②正确;
③酸溶液加水稀释,溶液中氢离子浓度减小,pH增大,所以不能判断酸的酸性强弱,故③错误;
④如果HF为强酸,常温下0.1mol/L的HF溶液的pH应为1,而该溶液的PH为2.3,说明HF部分电离是弱酸,故④正确;
⑤HF能与Na2CO3溶液反应,产生CO2气体说明HF的酸性比碳酸的强,不能说明HF是弱酸,故⑤错误;
⑥不能利用物质的溶解性来判断是否为弱电解质,HF与水能以任意比混溶与HF的酸性无关,故⑥错误;
故选D.
点评 本题考查了弱电解质的判断,题目难度不大,熟练掌握弱电解质的特征“部分电离”是解答本题的关键,侧重于考查学生的分析能力和应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 将40 g NaOH溶于水配成1 L溶液,其浓度为l mol•L-1 | |
| B. | 将22.4 L HC1溶于水配成1 L溶液,其浓度为lmol•L-1 | |
| C. | 1 L含2 mol K+的K2SO4溶液中K2SO4的浓度为1mol•L-1 | |
| D. | 将浓度为0.5 mol.L-l的NaNO3溶液100 mL恒温蒸发至50 mL,其浓度变为1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③④ | C. | ②④ | D. | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热,然后将气体生成物通入澄清石灰水,观察现象 | |
| B. | 向两种相同浓度的盐溶液中滴入稀盐酸,观察反应的剧烈程度 | |
| C. | 向两种相同浓度的盐溶液中滴入酚酞,观察颜色 | |
| D. | 向两种相同浓度的盐溶液中滴入氢氧化钡溶液,观察现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCOOH+H2O?HCOO-+H3O+ | B. | H2CO3+H2O?HCO3-+H3O+ | ||
| C. | CO32-+H2O?HCO3-+OH- | D. | HS-+H2O?S2-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与稀硫酸反应 Fe+2H+═Fe3++H2↑ | |
| B. | 氢氧化铝与足量盐酸反应 Al(OH)3+3H+═Al3++3H2O | |
| C. | 钠和冷水反应 Na+2H2O═Na++H2↑+OH- | |
| D. | 铜片与稀硝酸反应 Cu+NO3-+4H+═Cu2++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下134.4L N2 | B. | 66g CO2 | ||
| C. | 标准状况下90g H2O | D. | 6.02×1024个H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线:
)是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线: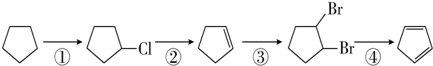
 ),途径如下:
),途径如下: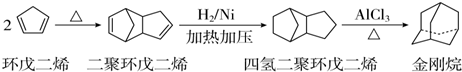
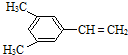 、
、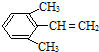 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com