
分析 (1)根据流程图中工业生产的原料,及发生的反应中的能量转化分析;
(2)沸腾炉中FeS2与氧气反应;根据生成磷肥的反应分析;
(3)根据FeS2制取硫酸过程中涉及的化学反应方程式,利用关系法解题;
(4)①石灰乳能将镁离子转化为沉淀;
②镁离子水解,应抑制其水解得到无水盐;
③用作镁蒸气的冷却剂,应不与Mg反应,以此来解答.;
(5)石灰石中的碳酸钙在高温条件下分解能生成氧化钙和二氧化碳,氧化钙能和二氧化硅反应生成硅酸钙,从而除去铁矿石中的二氧化硅.
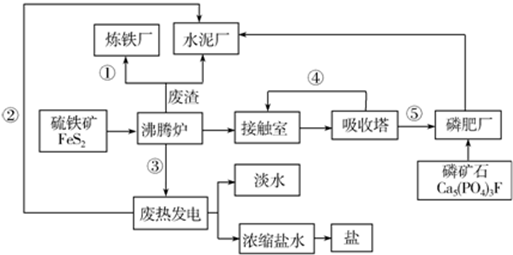
解答 解:(1)①中冶炼钢铁的原料是Fe2O3,②中热电厂中向外提供的能量为电能,③沸腾炉中FeS2与氧气反应放出大量的热,④制硫酸时接触室中二氧化硫被氧化,⑤硫酸工业中生成的硫酸,可用于制磷肥,
故答案为:①Fe2O3 ③热能 ④SO2 ;
(2)沸腾炉中FeS2与氧气反应生成Fe2O3和SO2,其反应方程式为:4FeS2+1102 $\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2;普钙是磷酸二氢钙和硫酸钙,用硫酸与磷酸钙反应生成硫酸钙和磷酸二氢钙的化学方程式为:Ca3(PO4)2+2H2SO4=Ca(H2PO4)2+2CaSO4,
故答案为:4FeS2+1102 $\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2;Ca3(PO4)2+2H2SO4=Ca(H2PO4)2+2CaSO4;
(3)FeS2制取硫酸过程中,设生成的98%的硫酸为x吨,利用关系法列式,硫元素守恒,
FeS2 ~2H2SO4
120 2×98
1×36%×65% 98%x
所以:$\frac{120}{1×36%×65%}$=$\frac{2×98}{98%x}$,得x=0.39,
故答案为:0.39;
(4)①石灰乳能将镁离子转化为沉淀,则在母液中加入石灰乳所起的作用是沉淀Mg2+,
故答案为:沉淀Mg2+;
②镁离子水解,应抑制其水解得到无水盐,所以利用MgCl2•6H2O制得无水氯化镁,应采取的措施是在HCl气流中脱水,抑制氯化镁水解,
故答案为:在HCl气流中脱水,抑制氯化镁水解;
③用作镁蒸气的冷却剂,应不与Mg反应,只有A符合,而Mg与二氧化碳、氧气、水蒸气等均可反应,
故答案为:A;
(5)石灰石中的碳酸钙在高温条件下分解能生成氧化钙和二氧化碳,氧化钙能和二氧化硅反应生成硅酸钙,从而除去铁矿石中的二氧化硅,
故答案为:碳酸钙.
点评 本题考查了工艺流程,涉及硫酸工业、水泥工业、磷肥工业、海水的应用等知识,内容较多,题目难度中等,注意根据对应的工业反应原理分析.


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ①②③④⑥ | C. | ①②③⑤ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| 选项 | 装置和操作 | 评价 |
| A | 用装置①量取15.00ml的NaOH溶液 | 错误:不能用酸式滴定管,应改用碱式滴定管 |
| B | 用装置②制备Cl2 | 错误:氯气密度大于空气,收集时导管应长进短出 |
| C | 用装置③验证溴乙烷发生消去反应生成烯烃 | 正确:生成的乙烯可使高锰酸钾褪色 |
| D | 关闭活塞a,从b处加水,以检查装置④的气密性 | 正确:b处加水后,左右液面形成稳定的高度差,证明气密性良好 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ | |
| B. | 用惰性电极电解CuCl2溶液:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$4H++O2↑+2Cu | |
| C. | 0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液体积混合NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 在酸性重铬酸钾溶液中加入少量乙醇3CH3CH2OH+2Cr2O72-+13H+→4Cr3++3CH3COO-+11H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 此时溶液中NH3•H2O的物质的量浓度为$\frac{a-0.01}{2}$+10-10-10-4mol/L | |
| B. | 溶液中c(NH4+)=c(Cl-) | |
| C. | 此时水的电离程度最大 | |
| D. | 25℃时NH3•H2O的电离平衡常数Kb=$\frac{{{{10}^{-9}}}}{a-0.01}$(mol/L) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 它是一种共价化合物 | |
| B. | 在加热时此化合物可以分解为 PH3和 HI 或 H2和 I2 | |
| C. | 这种化合物能跟碱反应 | |
| D. | 该化合物可以由 PH3 和 HI 化合而成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 在新生成的AgCl沉淀中滴入稀KI溶液,振荡 | 白色沉淀转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4, | 在管口观察到红棕色气体 | HNO3分解成了NO2 |
| C | 向CH3CH2X中加入少量AgNO3溶液,加热 | 有浅黄色沉淀生成 | CH3CH2X中含有Br- |
| D | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热, | 没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com