
分析 (1)钙的化学性质与钠相似,结合Na2O2与水的反应来分析;
(2)在反应中,钙元素的价态由0变为+2价,水的氢元素的价态由+1价变为0价,据此分析.
(3)根据钙与钠的性质的相似性来分析,仿照利用钠来制取过氧化钠的反应条件来书写;
(4)利用CaO2与Na2O2的性质的相似性来分析.
解答 解:(1)CaO2与Na2O2的性质的有很强的相似性,Na2O2与水的反应生成NaOH和O2,故CaO2和H2O反应生成Ca(OH)2和O2,故反应为2CaO2+2H2O═2Ca(OH)2+O2↑,
故答案为:2CaO2+2H2O═2Ca(OH)2+O2↑;
(2)在反应中,钙元素的价态由0变为+2价,1molCa失去2mol电子;水的氢元素的价态由+1价变为0价,2molH2O得2mol电子,故电子转移的方向和数目为: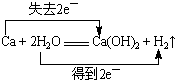
,故答案为: ;
;
(3)钙与钠的性质具有很强的相似性,用钠来制取过氧化钠的反应条件是加热,故以钙为原料制取过氧化钙(CaO2)也是将钙放在空气中加热即可,故反应为:
Ca+O2$\frac{\underline{\;加热\;}}{\;}$CaO2,
故答案为:Ca+O2$\frac{\underline{\;加热\;}}{\;}$CaO2;
(4)Na2O2与水反应时,先发生复分解反应生成H2O2和NaOH,然后H2O2分解生成氧气,故在Na2O2与水反应时即体现碱性也体现漂白性;而CaO2与Na2O2的性质有相似性,故在CaO2的水溶液中,也会先生成Ca(OH)2和H2O2,体现碱性也体现漂白性,故滴入酚酞溶液,预期的实验现象可能是溶液先变红色,后褪色;
故答案为:溶液先变红色,后褪色.
点评 本题考查了氧化还原反应、物质性质的相似性和递变性,难度不大,应根据钠及其化合物的性质来推测钙及其化合物的性质,注意把握双线桥表示电子转移的方法.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| B. | 1mol甲烷最多与2molCl2发生取代反应 | |
| C. | 标准状况下,2.24L乙醇含有的分子数目为0.1NA | |
| D. | 0.5 mol苯分子中含有C=C双键数为1.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L苯含有的分子数为0.1NA | |
| B. | 常温常压下,18g H2O含有10nA个电子 | |
| C. | 1L1mol•L-1的NH4Cl溶液中有nA个NH4+ | |
| D. | 一定条件下,向密闭容器中投入3mol H2和1mol N2充分反应后可得到NH3分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、ClO-、Cl- | B. | Mg2+、Na+、SO42-、Cl- | ||
| C. | Ca2+、HCO3-、NO3-、K+ | D. | Na+、Cu2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
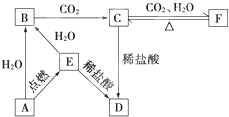
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将(CH3)3CCH2Cl与氢氧化钾的乙醇溶液加热一段时间后冷却,再滴加硝酸酸化的硝酸银溶液,可观察到有白色沉淀产生 | |
| B. | 新制氢氧化铜悬浊液可检验失去标签的乙醛、乙酸、乙酸乙酯(必要时可加热) | |
| C. | 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | |
| D. | 向淀粉溶液中加稀硫酸,加热几分钟,冷却后加入新制氢氧化铜悬浊液,若加热后未见砖红色沉淀生成,说明淀粉未开始水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com