
| O | 2-3 |
| O | 2-4 |
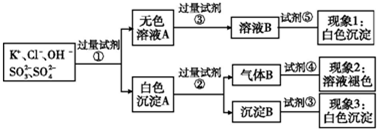
| A.试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl | ||
| B.现象3中白色沉淀是BaSO4 | ||
C.产生现象2的离子方程式是:Br2+2H2O+SO2=4H++2Br-+S
| ||
| D.试剂②是盐酸,试剂③是硝酸 |


科目:高中化学 来源:不详 题型:单选题
| A.溴苯中混有溴,加入KI溶液后,用分液漏斗分液 |
| B.除去乙烷中的乙烯,通入足量酸性KMnO4溶液中,再通入浓硫酸中 |
| C.溴乙烷中含有少量乙醇杂质,加入氢溴酸并加热,使乙醇转化为溴乙烷 |
| D.硝基苯中含有少量酸杂质,加氢氧化钠溶液振荡,静置分层后,用分液漏斗分离 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
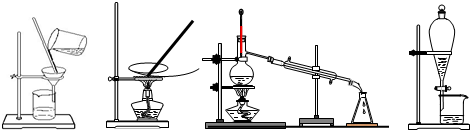
| A.过滤、蒸发、蒸馏、萃取 | B.过滤、蒸馏、蒸发、萃取 |
| C.蒸发、蒸馏、过滤、萃取 | D.萃取、蒸馏、蒸发、过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 2-4 |
| 2-3 |
| 2-3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| O | 2-3 |
| O | 2-4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 步骤 | 检验离子 | 检验方法 | 现象 | 离子方程式 |
| Ⅰ | ①______ | 焰色反应 | 火焰呈紫色(透过蓝色钴玻璃) | ______ |
| Ⅱ | Al3+ | 将氢氧化钠溶液逐滴加入到明矾溶液止过量 | ②先观察到: ______ | Al3++3OH-=Al(OH)3↓ |
| 后观察到: ______ | ③______ | |||
| Ⅲ | SO42- | ④先加______ | 无明显现象 | ______ |
| 后加______ | 产生白色沉淀 | Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com