
| A. | 0.533L | B. | 0.267L | C. | 4.0L | D. | 2.0L |
分析 根据MgCl2和AlCl3的混合溶液与碱的反应可知,要使Mg2+全部转化为沉淀分离出来,Al3+恰好转化为AlO2-,先利用电荷守恒来计算Al3+的浓度,再根据反应方程式计算即可.
解答 解:则将Mg2+、Al3+的物质的量分别为0.2L×2mol/L=0.4mol、0.2L×3mol/L=0.6mol,
由发生反应为MgCl2+2NaOH=Mg(OH)2↓+2NaCl
1 2
0.4mol 0.8mol
AlCl3+4NaOH=NaAlO2+3NaCl+2H2O,
1 4
0.6mol 2.4mol
使Mg2+全部转化为沉淀分离出来,消耗的NaOH的物质的量为0.8mol+2.4mol=3.2mol,
则需加4mol•L-1NaOH溶液的体积为$\frac{3.2mol}{0.8mol/L}$=4L,
故选C.
点评 本题考查离子的分离及利用化学反应方程式的计算,明确Mg2+全部转化为沉淀分离出来发生的化学反应是解答本题的关键,并注意利用氢氧化铝的两性来解答.


科目:高中化学 来源: 题型:选择题
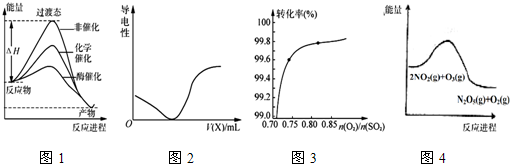
| A. | 由图1所示曲线可知,化学催化比酶催化的效果好 | |
| B. | 在H2S溶液导电性实验中,由图2所示曲线可确定通入的气体X为Cl2 | |
| C. | 其它条件不变,关于反应2SO2(g)+O2(g)$?_{加热}^{催化剂}$2SO3(g),图3中纵坐标表示O2的转化率 | |
| D. | 图4的反应升高温度,平衡常数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9种 | B. | 12种 | C. | 15种 | D. | 18种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素都是活泼的金属元素 | |
| B. | 卤素是常见的成盐元素,都是氧化剂 | |
| C. | 卤素原子最外层都有7个电子 | |
| D. | 卤化氢、卤化银的性质都有相似之处 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
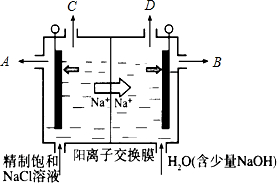 二氧化氯(ClO2)正逐步代替Cl2成为公认的高效、广谱、安全的水处理剂.当自来水厂用ClO2处理后水中含ClO2在0.1~0.8mg•L-1之间时,即达到合格标准.
二氧化氯(ClO2)正逐步代替Cl2成为公认的高效、广谱、安全的水处理剂.当自来水厂用ClO2处理后水中含ClO2在0.1~0.8mg•L-1之间时,即达到合格标准.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 8mL | B. | 10mL | C. | 15mL | D. | 23.75mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温、常压下,11.2L N2含有的分子数为0.5NA | |
| B. | 标准状况下,18g H2O的体积是22.4L | |
| C. | NA个SO2的体积是22.4L | |
| D. | 标准状况下,22.4L H2 与O2的混合气体所含原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com