
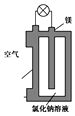
 镁与锂相比有多种优点,比如锂的熔点约为180摄氏度,而镁的熔点高达约650摄氏度,因而更为安全,镁的蕴藏量也比锂丰富得多.图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料.下列有关该镁燃料电池的叙述正确的是( )
镁与锂相比有多种优点,比如锂的熔点约为180摄氏度,而镁的熔点高达约650摄氏度,因而更为安全,镁的蕴藏量也比锂丰富得多.图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料.下列有关该镁燃料电池的叙述正确的是( )| A. | 圆筒为正极,电极反应式为O2+4e-═2O2- | |
| B. | 该电池的总反应为2Mg+O2+2H2O═2Mg(OH)2 | |
| C. | Cl-在阳极失去电子生成Cl2 | |
| D. | 在反应过程中消耗24g的镁,同时消耗空气的体积大约为11.2L(标准状况) |
分析 A、圆筒为正极,发生还原反应;
B、该电池的总反应式为镁、氧气和水反应生成氢氧化镁;
C、是原电池,氯离子未参与电极反应;
D、该电池的总反应为2Mg+O2+2H2O═2Mg(OH)2,每消耗2mol的镁反应的氧气在标况下的体积为22.4L.
解答 解:A、圆筒为正极,发生还原反应,电极反应式为O2+4e-+2H2O=4OH-,故A错误;
B、该电池的总反应式为镁、氧气和水反应生成氢氧化镁,电极反应式为:2Mg+O2+2H2O═2Mg(OH)2,故B正确;
C、是原电池,氯离子未参与电极反应,故C错误;
D、该电池的总反应为2Mg+O2+2H2O═2Mg(OH)2,每消耗2mol的镁反应的氧气在标况下的体积为22.4L,所以消耗24g的镁,同时消耗氧气的体积大约为11.2L,而不是空气,故D错误;
故选B.
点评 本题考查了原电池原理,明确正负极上发生的反应是解本题关键,结合放电顺序来分析解答,题目难度不大.


科目:高中化学 来源: 题型:实验题
 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
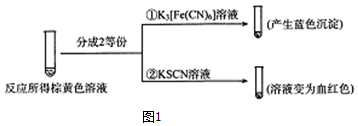
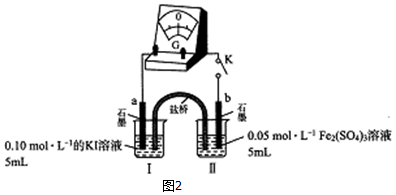
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 95%的酒精用于医疗中可作消毒剂,硫酸钡用于医疗中可作钡餐 | |
| B. | 食品中用木糖醇作甜味剂,可降低糖尿病的犯病几率 | |
| C. | 焊接废旧钢材前,分别用饱和Na2CO3溶液、NH4Cl溶液处理焊点 | |
| D. | 钙基固硫和NOx的催化转化都是解决空气污染问题的措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂是单位质量产生能量最高的营养物质 | |
| B. | 石油裂解的目的是提高轻质液体燃料的产量 | |
| C. | 钠钾合金密度小,熔点低,所以可用作核反应堆的传热介质 | |
| D. | 将苦卤浓缩、氧化,鼓入热空气和水蒸气可提取得到海水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL4mol/L的硫酸与足量Cu共热,转移的电子数为0.4NA | |
| B. | 1L 0.1mol•L-1的Na2CO3溶液中含有阳离子的总数为0.2NA | |
| C. | O2和O3的混合物共3.2g,其中所含氧原子数一定为0.2NA | |
| D. | 室温时,pH=12的Ba(OH)2溶液中,氢氧根离子数目为10-2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用灼烧的方法可以区分羊毛和人造纤维 | |
| B. | 医用消毒酒精是体积分数为95%的乙醇 | |
| C. | 食用一定量的油脂能促进人体对某些维生素的吸收 | |
| D. | 加热能杀死流感病毒是因为蛋白质受热变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4L NO和11.2L O2在密闭容器中充分反应后,总分子数小于NA | |
| B. | 28g C2H4和C3H6的混合物含有C-H键数目为4NA | |
| C. | 标准状况下,22.4L Cl2与适量H2O或NaOH反应转移的电子数目都为NA | |
| D. | 常温下,1L pH=13的Ba(OH)2中OH-的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
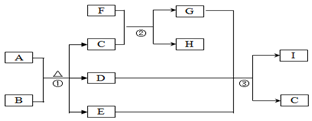 有关物质的转化关系如图所示(部分生成物与反应条件已略去).A是常见的非金属固体单质,F是紫红色的金属单质,B、C是常见的强酸,D、G、I是常见的气体,D与I的组成元素相同,且D的相对分子质量比I的大16.E是最常见的无色液体.
有关物质的转化关系如图所示(部分生成物与反应条件已略去).A是常见的非金属固体单质,F是紫红色的金属单质,B、C是常见的强酸,D、G、I是常见的气体,D与I的组成元素相同,且D的相对分子质量比I的大16.E是最常见的无色液体. .
. 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com