
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
分析 铁棒与石墨棒用导线连接后浸入0.01mol•L-1的食盐溶液中,构成原电池,Fe为负极,石墨为正极,发生吸氧腐蚀,以此来解答.
解答 解:铁棒与石墨棒用导线连接后浸入0.01mol•L-1的食盐溶液中,构成原电池,Fe为负极,石墨为正极,发生吸氧腐蚀,
①碳棒上氧气得电子生成氢氧根离子,没有氢气析出,故错误;
②碳棒上氧气得电子生成氢氧根离子,即碳棒附近产生OH-,故正确;
③中性条件下,发生吸氧腐蚀,故错误;
④电解质溶液为NaCl溶液,显中性,中性条件下发生吸氧腐蚀,故正确;
故选D.
点评 本题考查了原电池原理和吸氧腐蚀,明确电极的判断及发生的电极反应即可解答,题目难度不大,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 两个电极均为铁片,M是阴极,电解质溶液是0.4%的NaOH溶液 | |
| B. | 两个电极均为石墨,M是阳极,电解质溶液是0.4%的H2SO4溶液 | |
| C. | M是铁片,作阴极,N是石墨,电解质溶液是0.4%的Ba(NO3)2溶液 | |
| D. | M是铁片,作阴极,N是石墨,电解质溶液是0.4%的HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
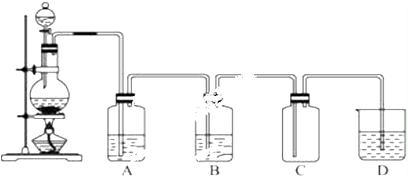
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
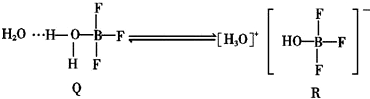
| A. | 离子键 | B. | 配位键 | C. | 非极性共价键 | D. | 氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
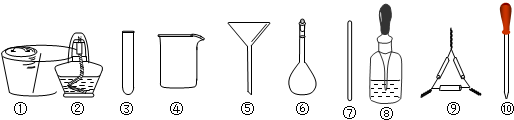
| A. | 将茶叶灼烧灰化,选用①、②和⑨ | |
| B. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ | |
| C. | 过滤得到滤液,选用④、⑤和⑦ | |
| D. | 检验滤液中的Fe3+,选用③和⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
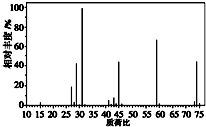 根据以下有关信息确定有机物的组成
根据以下有关信息确定有机物的组成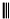 +
+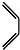 $\stackrel{△}{→}$
$\stackrel{△}{→}$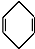 如果要合成
如果要合成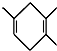 ,所用的起始原料的结构简式为C(CH3)2=C(CH3)2、CH3C≡CH或CH2=C(CH3)-CH=CH2、CH3C≡CCH3.
,所用的起始原料的结构简式为C(CH3)2=C(CH3)2、CH3C≡CH或CH2=C(CH3)-CH=CH2、CH3C≡CCH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ②③④⑥ | C. | ①③④⑤ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| v正 | v逆 | 平衡常数K | 转化率α |
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com