
已知:常温下浓度均为0.1 mol/L的下列溶液的pH如表:
溶质 | NaF | Na2CO3 | NaClO | NaHCO3 |
pH | 7.5 | 11.6 | 9.7 | 8.3 |
下列有关说法正确的是( )
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B.等体积等物质的量浓 度的NaClO溶液与NaF溶液中离子总数大小:N前<N后
度的NaClO溶液与NaF溶液中离子总数大小:N前<N后
C.若将CO2通入0. 1mol/LNa2CO3溶液至溶液中性,则溶液中:2c(CO32-)+c(HCO3-)=0.1mol/L
1mol/LNa2CO3溶液至溶液中性,则溶液中:2c(CO32-)+c(HCO3-)=0.1mol/L
D.向Na2CO3溶液中通入少量的HF气体,化学反 应方程式为:Na2CO3+2HF=CO2+H2O+2NaF
应方程式为:Na2CO3+2HF=CO2+H2O+2NaF
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源:2017届安徽省六校教育研究会高三上第一次联考化学卷(解析版) 题型:选择题
如图,用下列实验操作可完成两个实验。甲实验为粗盐中难溶性杂质的去除,乙实验为配制溶质的质量分数为10%的氯化钠溶液。下列说法中正确的是
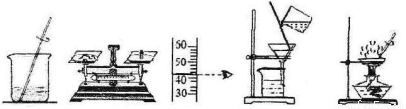
① ② ③ ④ ⑤
A.甲实验的步骤是①④⑤,其中去除杂质的关键步骤是蒸发
B.甲实验各步操作中,玻璃棒的作用都是相同的
C.乙实验若按照②③①的步骤进行操作,砝码为5g(游码读数0),则配制的溶液浓度偏大(p水=lg/cm3)
D.乙实验中,若①所用的烧杯内璧沾有水,对配制的溶液浓度无影响
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一11月月考化学卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列叙述正确的是
A.将足量Na、Mg、A1分别投入到含0.5 mol的HCl的溶液中,转移电子数均为0.5 NA
B. 将lmolCO2、H2O蒸气混和物通过足量Na2O2,气体分子数变为0.5 NA
C.将含有1mol Na2CO3的溶液逐滴加入到含1.5molHCl的溶液中,产生气体分了数目为0.5NA个
D. 1molNa2O2与足量CO2反应转移的电子数为2NA个
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:填空题
(1) 加热蒸干Al2(SO4)3溶液,得到的固体物质是 (写化学式)。
(2) 加热蒸干NaHCO3溶液,得到的固体物质是 (写化学式)。
(3) 加热蒸干Na2SO3溶液,得到的固体物质是 (写化学式)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:选择题
分子式为C8H18的烷烃中,含有4个甲基的同分异构体的数目是( )
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:选择题
常温下,下列溶液:① pH=14的NaOH溶液,② 0.5 mol/L的NaOH溶液,③ 0.1 mol/L的Na2CO3溶液,④ 0.1 mol/L的KHCO3溶液,⑤ 0.1mol/L的HNO3溶液。 其中由水电离出的c(OH-)由大到小的顺序为: ( )
其中由水电离出的c(OH-)由大到小的顺序为: ( )
A.③④⑤①② B.①②⑤③④ C.⑤④③②① D.③④⑤②①
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第三次质检化学试卷(解析版) 题型:实验题
新切开的苹果在空气中放置一段时间表面会变黄,最终变成褐色,这种现象在食品科学上通常称为“褐变”。 关于苹果褐变的原因有以下两种说法:为____________
A.苹果中的Fe2+被空气中的氧气氧化成了Fe3+
B.苹果中的酚类物质被空气中的氧气氧化了
究竟哪种说法正确,某小组同学通过实验进行了探究。
实验用品:苹果、浓度均为0.1mol·L-1的盐酸、NaHCO3溶液、Na2SO3溶液,KSCN溶液,去氧蒸馏水。
(1)探究1:
实验操作 | 实验现象 | 结论 |
在“褐变”后的苹果上滴上2~3滴 溶液。 | _________________ | 说法A不正确 |
(2)探究2:【查阅文献】Ⅰ.苹果中含有多种酚和酚氧化酶,苹果中酚氧化酶的活性温度为35℃左右、活性pH约为5.5-7.5。Ⅱ.酚类物质遇FeCl3溶液常发生显色反应而呈现一定颜色,如苯酚显紫色,对苯二酚显绿色,甲基苯酚显蓝色。
该小组将刚削皮的苹果切成七块,分别进行如下实验。请填写下表中相应的结论:
序号 | 实验步骤 | 现 象 |
|
① | 在一块上滴加2至3滴FeCl3溶液 | 表面变为绿色 | ______________ |
② | 再取两块,一块放置于空气中,另一块迅速浸入经过去氧的蒸馏水中。 | 前者表面逐渐褐变,后者相当长一段时间内,无明显变化。 | 苹果褐变与_________有关 |
③ | 另两块分别立刻放入沸水和0.1mol·L–1盐酸中浸 | 相当长一段时间内,两块均无明显变化。 | 苹果褐变与酚氧化酶的活性有关 |
④ | 最后两块分别立刻放入浓度均为0.1mol·L–1的NaHCO3和Na2SO3溶液里浸泡2min后取出,置于空气中。 | 前者经过一段时间表面逐渐褐变,后者相当长一段时间内,无明显变化。 | 亚硫酸钠溶液能阻止苹果褐变 |
(3)问题分析:Ⅰ、常温下,浓度均为0.1 mol· L-1 NaHC O3溶液略显碱性,而NaHSO3溶液却略显酸性。 NaHSO3溶液略显酸性是因为 。
O3溶液略显碱性,而NaHSO3溶液却略显酸性。 NaHSO3溶液略显酸性是因为 。
Ⅱ、0.1mol· L–1的NaHCO3溶液和Na2SO3溶液的pH相近,Na2SO3溶液却能阻止苹果褐变,结合离子方程式分析原因 : 。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第三次质检化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.室温下,1L pH=1的盐酸中,由水电离的H+离子数目为0.1NA
B.标况下,11.2L NO2 所含的分子数目为0.5 NA
C.甲烷碱性燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA
D.1 mol C2H6O分子中含有的O—H键数目一定为NA
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第三次周考化学卷(解析版) 题型:选择题
某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是
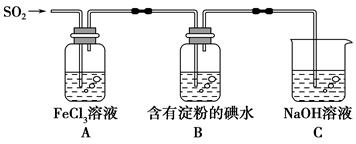
A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液退色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色退去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com