
| A. | 在周期表中,元素的族序数都等于其原子的最外层电子数 | |
| B. | 周期表中非金属性最强的元素,其最高价氧化物的水化物酸性也最强 | |
| C. | 同主族元素随原子核电荷数的递增,原子半径依次增大 | |
| D. | 第ⅦA族元素的单质,随分子量的增大,熔、沸点升高;ⅠA族单质,随分子量的增大,熔、沸点升高 |
分析 A.主族元素的族序数等于最外层电子数;
B.周期表中非金属性最强的元素,为F,没有正价;
C.同主族从上到下原子半径增大;
D.ⅠA族碱金属单质,随原子序数增大,熔沸点降低.
解答 解:A.主族元素的族序数等于最外层电子数,副族元素不一定,故A错误;
B.周期表中非金属性最强的元素,为F,没有正价,则不存在最高价氧化物的水化物,故B错误;
C.同主族从上到下原子半径增大,则同主族元素随原子核电荷数的递增,原子半径依次增大,故C正确;
D.ⅠA族碱金属单质,随原子序数增大,熔沸点降低,而第ⅦA族元素的单质,随分子量的增大,熔、沸点升高,因晶体类型及作用力不同,故D错误;
故选C.
点评 本题考查周期表和周期律的应用,为高频考点,把握原子结构与元素的位置、元素的性质、元素周期律等为解答的关键,侧重分析与应用能力的考查,注意D中性质比较方法,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
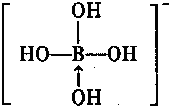 .(若存在配位键需标出)
.(若存在配位键需标出)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
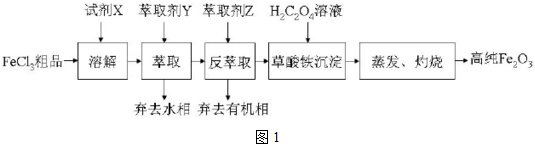
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
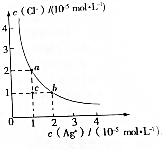
| A. | a点和b点对应的Ksp(AgCl)相等 | |
| B. | Ksp(AgCl)=2×10-10 | |
| C. | 可采取蒸发溶剂的方法使溶液从c点变到b点 | |
| D. | 已知Ksp(AgI)=8.5×10-17,向含KI和KCl的溶液中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$=4.25×10-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
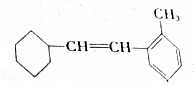 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
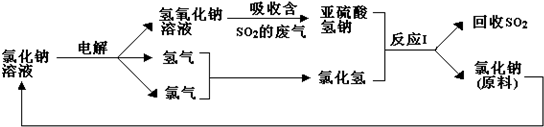
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的原子半径、失电子能力随核电荷数的增加而增大 | |
| B. | 被其它卤素单质从其卤化物中置换出来的可能性随核电荷数的增加而增大 | |
| C. | 它们的氢化物的稳定性随核电荷数的增加而增强 | |
| D. | 单质的颜色随核电荷数的增加而加深 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com