
| A. | 氯水 | B. | 乙烯 | C. | 乙醇 | D. | 碘化钾溶液 |
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Na+>N3->H+ | |
| B. | 氢铝化合物与水反应生成氢氧化铝和氢气 | |
| C. | 与盐酸反应都只生成一种盐 | |
| D. | 与水反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
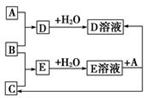 已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图框图进行反应.
已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图框图进行反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④①③ | B. | ③④①② | C. | ①②④③ | D. | ②①④③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
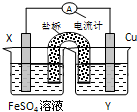
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
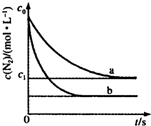
| A. | 曲线a和曲线b表示该反应可能在相同温度下进行 | |
| B. | 曲线b对应的起始反应条件改变是加入了催化剂 | |
| C. | 温度T下,该反应平衡前后混合气体的密度不发生变化 | |
| D. | 温度T下,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{C}_{0}}^{2}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
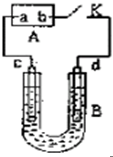 如图,A为直流电源,B为电解槽,c、d为石墨电极,B中存放有100mL NaCl和CuCl2的混合溶液,其中Cu2+的物质的量浓度为0.1mol/L,闭合K,d极收集到标准状况下448mL的一种气体甲,该气体能使湿润的碘化钾淀粉试纸变蓝.气体体积均在标准状况下测定,假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收.请回答下列问题.
如图,A为直流电源,B为电解槽,c、d为石墨电极,B中存放有100mL NaCl和CuCl2的混合溶液,其中Cu2+的物质的量浓度为0.1mol/L,闭合K,d极收集到标准状况下448mL的一种气体甲,该气体能使湿润的碘化钾淀粉试纸变蓝.气体体积均在标准状况下测定,假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠用于潜艇供氧 | B. | 氧化铁用做红色颜料 | ||
| C. | 在海轮的外壳上焊接铜板防腐 | D. | 铝制槽车可用来储运浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com