
下列各组离子在指定溶液中,能大量共存的是 ( )
①无色溶液中:K+,Cl-,Ca2+,CO33-,SO42-,NO3-
②pH=11的溶液中:CO32-,Na+,[Al(OH)4]-,NO3-,S2-,SO32-
③水电离的H+浓度c(H+)=10-12mol·L-1的溶液中:Cl-,CO32-,NO3-,NH4+,SO32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使石蕊变红的溶液中:Fe2+,MnO4-,NO3-,Na+,SO42-
⑥中性溶液中:Fe3+,Al3+,NO3-,I-,Cl-,S2-
A.①②⑤ B.①③⑥ C.②④ D.①②④
科目:高中化学 来源: 题型:
工业上制备BaCl2的工艺流程图如下:
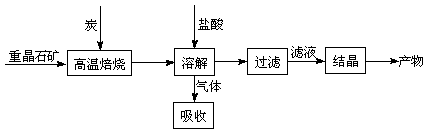
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaS O4(s) + 4C(s)
O4(s) + 4C(s) 4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,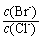 = 。
= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g) 2CO(g)的△H2= kJ·mol-1。
2CO(g)的△H2= kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如右下图所示的装置制取乙酸乙酯,请回答下列问题。
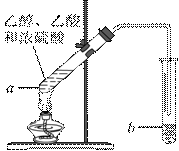 (1)乙醇分子中官能团的名称是________________。
(1)乙醇分子中官能团的名称是________________。
(2)试管a中加入几块碎瓷片的目的是_________。
(3)试管a中发生反应的化学方程式为
___________________________________________,
反应类型是____________________。
(4)反应开始前,试管b中盛放的溶液是____________。
(5)可用____________的方法把制得的乙酸乙酯分离出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E均为有机物,它们具有下图的转化关系:
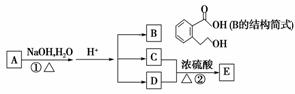
已知:C能与NaHCO3发生反应,C、D相对分子质量相等,E能发生银镜反应,相对分子质量为74。
请回答下列问题:
(1)写出C的名称:________,E中含有的官能团(写结构简式)________、________;写出有机物B可能发生的两种反应类型:_______________________;
(2)写出反应②的化学方程式:_____________________________________;
该反应需加热的目的是___________________________________________;
(3)A的结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时。已知下表数据
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的PH值 | ≥9.6 | ≥6.4 | 3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是 ( )
A. 向该溶液中加少量铁粉即能观察到红色固体析出
B. 该溶液中c(SO42-):{c(Cu2+)+c(Fe2+)+c(Fe3+)}>5:4
C. 向该混合溶液中逐滴加入NaOH溶液,最新看到红褐色沉淀
D. 向该溶液中加入适量氯水,并调节pH值到3~4后过滤,得到纯净的CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。工业上制备K2FeO4的常用方法有两种。
方法Ⅰ:次氯酸盐氧化法。工艺流程如下图所示。
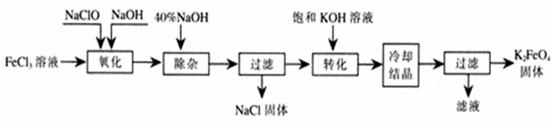
⑴ 写出“氧化”过程中反应的化学方程式: 。
⑵写出“转化”过程中发生反应的化学方程式为 。
⑶上述工艺得到的高铁酸钾常含有杂质,可用重结晶发提纯,操作是:将粗产品用 溶解,然后 。
方法Ⅱ:电解法。以铁为阳极电解氢氧化钠溶液,然后在阳极溶液中加入KOH。
⑷电解时阳极发生反应生成FeO42-,该电极反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,完全燃烧时生成水的质量和消耗氧气的质量就不变的是( )
A.C3H6,C4H8 B.C3H6,C4H6O C.C2H6,C3H6O2 D.CH4O,C3H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时,合成氨反应N2(g)+3H2(g) 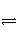
 2NH3(g)
2NH3(g)
ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为23 kJ(假定测量过程中没有能量损失),则N2的转化率为( )
A.25% B.50% C.75% D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com