
【题目】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次增大,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层龟子数是次外层电子数的3倍。
(1)试推断它们各是什么元素? 写出它们的元素符号:A______,B________,C_______,D_______。
(2)甲、乙、丙、丁是由以上四种元素中的几种组成的10 电子微粒;
①甲为分子,且能刻蚀玻璃,则甲的化学式为______
②乙为气体,且遇到无色酚酞溶液变成红色,则乙的化学式为_______
③丙为阳离子,丁为阴离子,且丙和丁在加热条件下生成的两种物质也是10电子微粒,请写出该反应的离子方程式_______________。
【答案】 H C N O HF NH3 NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
【解析】考查元素周期表和元素周期律的应用,A原子核内仅有一个质子,推出A为H,D原子有两个电子层,最外层电子数是次外层电子数的3倍,即D为O,B原子的电子总数与D原子的最外层电子数相等,即B为C,A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,即C为N,(1)根据上述分析,A为H,B为C,C为N,D为O;(2)①甲分子能刻蚀玻璃,工业上常用氢氟酸刻蚀玻璃,因此甲为HF;②乙为气体,能使无色酚酞溶液变红,说明乙气体溶于水显碱性,即乙为NH3;③根据10电子微粒,发生的离子反应是NH4++OH-![]() NH3↑+H2O。
NH3↑+H2O。


科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.AlCl3溶液中通入过量的氨水:Al3++4NH3·H2O=AlO2-+2H2O+4NH4+
B.向NH4 HCO3溶液中加过量NaOH 溶液并加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
C.将Cu片加入稀硝酸中:3Cu+8H++2NO3- =3Cu2++2NO↑+4H2O
D.向Na2S2O3溶液中加入稀硫酸:2S2O32—+2H+=SO42—+3S↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中能够大量共存的是( )
A.Na+、Cl﹣、NO3﹣
B.Ag+、Cl﹣、NO3﹣
C.NH4+、OH﹣、SO42﹣
D.Na+、Fe2+、OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)粗制CuSO45H2O晶体中常含有杂质Fe2+ . ①在提纯时为了除去Fe2+ , 常加入合适氧化剂,使Fe2+氧化为Fe3+ , 下列物质最好选用的是 .
A.氯水 B.HNO3 C.KMnO4 D.H2O2
②然后再加入适当物质调整溶液至pH=4,使Fe3+转化为Fe(OH)3 , 调整溶液pH可选用下列中的 .
A.CuOB.Cu(OH)2 C.NaOH D.NH3H2O
(2)在25℃下,向浓度均为0.1molL﹣1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式为 . 已知25℃时Ksp[Mg(OH)2]=1.8×10﹣11 , Ksp[Cu(OH)2]=2.2×10﹣20 .
(3)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, ![]() = . [Ksp(AgBr)=5.4×10﹣13 , Ksp(AgCl)=2.0×10﹣10].
= . [Ksp(AgBr)=5.4×10﹣13 , Ksp(AgCl)=2.0×10﹣10].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.A、B、C、D均为中学化学常见的纯净物,A是单质,它们之间有如下的反应关系;
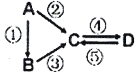
(1)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染,B与C在一定条件下反应生成的A是大气的主要成分,写出B-C的化学方程式:_______________。
(2)若D物质具有两性,②、③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体,写出A→C的离子方程式:______________________。
(3)若A是制作芯片常用材料,B为A单质的氧化物,C为水玻璃的主要成分.写出A→C的离子方程式:__________________________。
(4)若A是应用最广泛的金属.④反应用到A,②、⑤反应均用到同一种非金属单质,C的溶液用于蚀刻印刷铜电路板,写出C→D的离子方程式:__________________。
(5)若A为淡黄色固体,C、D是氧化物,且是是造成酸雨的主要物质,B与C可反应生成A。写出B完全燃烧的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,CaSO4的沉淀溶解平衡曲线如图,Ksp(CaSO4)=9×10﹣6 . 下列判断错误的是( ) 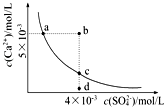
A.a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液
B.a点对应的Ksp等于c点对应的Ksp
C.b点将有沉淀生成,平衡后溶液中c(SO ![]() )一定等于3×10﹣3 mol?L﹣1
)一定等于3×10﹣3 mol?L﹣1
D.向d点溶液中加入适量CaCl2固体可以变到c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.右图为RFC工作原理示意图,有关说法正确的是( ) 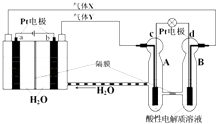
A.转移0.1mol电子时,a电极产生1.12LH2
B.b电极上发生还原反应
C.酸性电解质溶液中H+移向c电极
D.d电极上发生的电极反应是:O2+4H++4e﹣=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的同学为了探究原电池工作的原理,进行了如下系列实验,请你一起参与实验并分析实验结果后回答有关问题: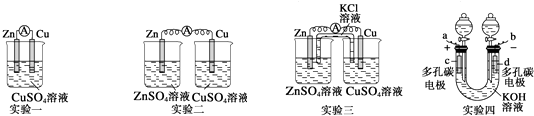
(1)实验一中铜片、锌片表面均有红色物质析出,电流计指针偏转,但较短时间内电流即明显减小.实验结束时测得锌片减少了3.94g,铜片增重了3.84g,则该原电池的工作效率是(指参加原电池反应的锌占反应总量的百分数).
(2)实验二中刚将铜、锌片插入溶液中时电流计指针有偏转,但立即就归零了.解释锌失去的电子能不能持续通过导线流向铜极给Cu2+ .
(3)实验三中盐桥中的K+流向溶液(填ZnSO4或CuSO4),如果Zn的消耗速率为1×10﹣3 mol/s,则K+的迁移速率为mol/s.
(4)实验四中,调节低压电源的电压到6V,并把其正、负极分别与上图装置中的两个碳电极相连接;接通电源,图示中的“+”连接到电源的正极上,“﹣”连接到电源的负极上,电解氢氧化钾溶液制取氢气、氧气,且制得的氢气与氧气的体积比为2:1,去掉电源,该装置就成为一只氢氧燃料电池,用带有一小灯泡的导线连接a、b,灯泡即可发亮.则下列说法错误的是 .
A.在电解KOH溶液制备H2和O2时,KOH的作用是增强溶液的导电性,一段时间后其浓度增大
B.当作为氢氧燃料电池时,c极发生氧化反应,d极发生还原反应
C.当作为氢氧燃料电池时,电解质溶液中的OH﹣向着d极移动
D.如将KOH溶液换成稀H2SO4 , 且作为氢氧燃料电池时,c极的电极反应为:O2+2H2O+4e﹣═4OH﹣ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com