
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度都相等时,下列说法正确的是( )
A.两种气体的压强相等
B.O2比O3的质量小
C.两种气体的分子数目相等
D.两种气体的氧原子数目相等
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:2017届河北武邑中学高三上学期周考(8.21)化学试卷(解析版) 题型:选择题
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径在36~55nm的磁流体。下列说法中正确的是( )
A.所得的分散系属于悬浊液 B.该分散系能产生丁达尔效应
C.所得的分散系中分散质为Fe2O3 D.分散系为胶体,且胶粒直径即Fe(OH)3分子直径
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南长沙市新高一分班考试化学(解析版) 题型:选择题
如下图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子。下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子。下列各项中对图示模型理解正确的是( )
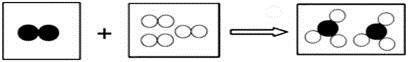
A. 该反应属于分解反应 B. 反应中共有两种元素参与
C. 反应物和生成物中只有一种单质 D. 参加反应的两种物质分子个数之比为2:3
查看答案和解析>>
科目:高中化学 来源:2017届江西省、宜春一中高三7月联考化学试卷(解析版) 题型:选择题
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mL B.45mL C.30mL D.无法计算
查看答案和解析>>
科目:高中化学 来源:2017届江西省、宜春一中高三7月联考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-===CaCO3↓+H2O
B.明矾溶液中滴加Ba(OH)2溶液至SO42-恰好完全沉淀:
Al3++Ba2++SO42-+3OH-===BaSO4↓+Al(OH)3↓
C.将过量SO2通入冷氨水中:SO2+NH3·H2O===HSO3-+NH4+
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO-+2Fe(OH)3===2FeO42-+3Cl-+H2O+4H+
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第一次月考(开学考试)化学(解析版) 题型:实验题
(10分)常温下,现有A、B、C、D四种电解质分别完全溶于水,所得四种溶液中含H+、Ba2+、Al3+、Na+、HCO3-、Cl-、OH-、SO42-八种离子(不考虑水解)。为了检验这四种物质,进行如下实验:
①取少量A的溶液分别与另三种物质反应,依次观察到:白色沉淀和气体、气体、白色沉淀。
②经测定,A和D的溶液显碱性,B和C的溶液pH<7。B与D的溶液反应产生两种沉淀,当D的量增大时,其中一种沉淀不断溶解,最终还存在一种沉淀。
③C与D的溶液反应,无明显现象。经测定,该反应的产物总能量小于反应物总能量。
根据上述实验事实,请回答下列问题:
(1)C的名称是________,D的化学式_________。
(2)用离子方程式表示A的溶液显碱性的原因:_________________。
(3)A与B在溶液中反应的离子方程式为________________。
(4)等物质的量浓度、等体积的B和D的溶液混合,写出反应的离子方程式:_________________。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第一次月考(开学考试)化学(解析版) 题型:选择题
20℃时,饱和NaCl溶液的密度为ρg·cm-3,物质的量浓度为cmol·L-1则下列说法中错误的是( )
A.温度低于20℃时,饱和NaCl溶液的浓度小于cmol·L-1
B.20℃时,饱和NaCl溶液的质量分数为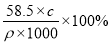
C.20℃时,密度小于ρg·cm-3的NaCl溶液是不饱和溶液
D.20℃时,饱和NaCl溶液的溶解度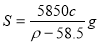
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:实验题
(10分)
(1)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
①Fe2O3(Al2O3) ②NaHCO3(Na2CO3)
③Cl2 (HCl) ④SiO2 (Fe2O3)
(2)将铁粉、铜粉、FeCl3溶液和CuCl2溶液混合于某容器中充分反应(容器不参与反应)。试判断下列情况下,溶液中存在的金属离子和金属单质。
①若铁粉有剩余,则容器中不可能有的离子是________________;铜单质________(填“一定”或“可能”)存在。
②若氯化铜有剩余,则容器中还可能有的离子为________;铜单质__________(填“一定”或“可能”)存在。
③若氯化铁和氯化铜都有剩余,则容器中不可能有的单质是______,Fe2+_______(填“一定”或“可能”)存在。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省大连市高二下期末化学试卷(解析版) 题型:推断题
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期.
(1)F 原子基态的外围核外电子排布式为 ;
(2)由A、B、C形成的离子CAB﹣与AC2互为等电子体,则CAB﹣的结构式为 ;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为 ;
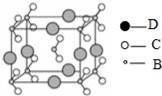
(4)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为 ;
(5)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2═CHCHO、HCOOH、CH3COONO2(PAN)等二次污染物.
①下列说法正确的是 ;
A.N2O为直线型分子
B.C、N、O的第一电离能依次增大
C.CH2═CH一CHO分子中碳原子均采用sp2杂化
D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4该配合物中心离子的配体为 ,其中提供空轨道的是 (填微粒符号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com