
广口瓶是中学实验中常用仪器之一,下列各装置中均有广口瓶,请填空:
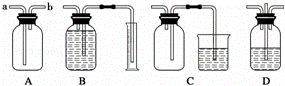
(1)装置A可用于收集气体,如H2,若装置A是干燥的,则气体应从 口进入(填“a”或“b”,下同),若A中充满水,则气体应从 口进入.
(2)装置B通常用于 ,注意事项是 .(写出两条)
(3)装置C的用途是 .
(4)装置D中长导管的作用是 ) .
考点:
实验装置综合;气体的净化和干燥.
专题:
实验题.
分析:
(1)氢气密度小于空气,应该使用向下排空气法,导管采用“短进长出”方式;排水法水解,应该采用“短进长出”方式;
(2)装置B通常用于排水法测量难溶性的气体体积;排水法测量气体体积时量筒中液面必须与集气瓶中液面相平,读取量筒中液体体积时要平视刻度线;
(3)装置C可以防止烧杯中的液体进入反应装置、且能够吸收尾气;
(4)装置D中的长导管可以使集气瓶中的气压与大气压相同.
解答:
解:(1)装置A可用于收集氢气时,氢气的密度比空气小,应该采用短进长出的方法,即从b口进入;排水法收集气体时应该采用短进长出方法,即从b口进入,
故答案为:b;b;
(2)装置B通常用于测量难溶气体的体积,在使用排水法测量气体体积时,读数时量筒中液面必须与集气瓶中液面相平;读取量筒中排出的水的体积时,眼睛与量筒刻度线、液面都相平,
故答案为:测难溶气体的体积;两侧液面相平、平视刻度线;
(3)装置C问问尾气吸收装置,装置C还具有防止倒吸的作用,
故答案为:尾气处理并防止倒吸;
(4)装置中的长导管能够使集气瓶内的气压与大气压相等,具有平衡气压的作用,还可以通过长导管判断装置是否通畅,
故答案为:平衡气压或观察是否通畅.
点评:
本题考查了常见装置的用途、连接方法,题目难度中等,注意常见装置的连接方法及用途,能够按照题干要求连接出具有相应功能的装置.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
两种气态烃以任意比例混合,在105℃时1L该混合烃与3L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是4L.下列各组混合烃中符合此条件的是( )
|
| A. | CH4、C2H4 | B. | CH4、C3H6 | C. | C2H4、C3H8 | D. | C2H2、C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在如图所示的一些常见单质、化合物等物质之间的转化关系中(有些反应的条件和部分物质未全部列出),已知在常温常压下,F为红棕色气体;L为白色不溶于水的固体,它既能与盐酸反应又能与氢氧化钠反应;G是硝酸;J是无色气体,且能够使燃着的木条熄灭;A为金属单质,其氧化物具有两性;D为非金属气态单质,是大气中含量最多的物质;H为非金属固态单质,其原子核中有6个质子.

(1)化合物C的化学式为 .
(2)物质I在生产生活中的用途有 (任答一条).
(3)写出E+氧气→F的化学方程式: .
(4)写出A与稀盐酸反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
|
| A. | 原子半径:W>Z>Y>X |
|
| B. | 最高价氧化物对应水化物的酸性:Z>W>X |
|
| C. | 四种元素的单质中,W单质的熔、沸点最高 |
|
| D. | W的单质能与水反应,生成一种具有漂白性的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式C8H8O2.A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如图.关于A的下列说法中,正确的是( )
|
| A. | 1molA在碱性条件下水解消耗2molNaOH |
|
| B. | A在一定条件下可与4 mol H2发生加成反应 |
|
| C. | 符合题中A分子结构特征的有机物只有1种 |
|
| D. | 与A属于同类化合物的同分异构体只有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
取一定量的铁、铜混合物粉末,平均分成五等份,分别向每一份中加入一定量的稀硝酸,实验中收集到的NO气体(稀硝酸的唯一还原产物)的体积及所得剩余固体的质量记录如下(所有气体的体积均在标况下测定)
| 实验序号 | 1 | 2 | 3 | 4 | 5 |
| HNO3溶液的体积(mL) | 100 | 200 | 300 | 400 | 500 |
| 剩余固体质量(g) | 17.2 | 8 | 0 | 0 | 0 |
| 气体体积(L) | 2.24 | 4.48 | 6.72 | 7.84 | 7.84 |
(1)该实验中所用硝酸的物质的量浓度
(2)第一次实验后剩余固体为 ,第二次实验剩余固体为 (均填写化学式)
(3)求实验中每次所取混合物中铜的质量 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A. NaAlO2溶液中通入过量的CO2:2AlO2﹣+3H2O+CO2═2Al(OH)3↓+CO32﹣
B. 明矾溶液中滴加Ba(OH)2溶液至SO42﹣完全沉淀:Al3++Ba2++SO42﹣+3OH﹣═BaSO4↓+Al(OH)3↓
C. 200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br﹣+5Cl2═4Fe3++3Br2+10Cl﹣
D. 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO﹣+2Fe(OH)3═2FeO42﹣+3Cl﹣+H2O+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
某待测溶液(阳离子为Na+)中可能含有SO42﹣、SO32﹣、NO3﹣、Cl﹣、Br﹣、CO32﹣、HCO3﹣中的一种或多种,进行如图所示的实验,每次实验所加试剂均过量,下列说法不正确的是( )
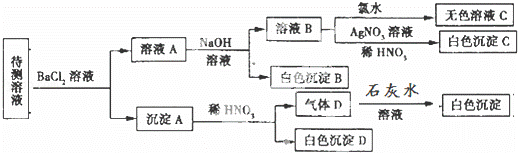
A. SO42﹣、SO32﹣至少含有一种
B. 沉淀B的化学式为BaCO3
C. 肯定存在的阴离子有CO32﹣、HCO3﹣、Cl﹣,还有SO42﹣、SO32﹣至少含有一种
D. 肯定没有的离子是Br﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
|
| A. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
|
| B. | 氢氧化铜可溶于氨水说明氢氧化铜是两性氢氧化物 |
|
| C. | 在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3给出孤电子对 |
|
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤电子对,NH3提供空轨道 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com