
| A. | ①②⑤⑥ | B. | ②③④⑤ | C. | ①③④⑤⑦ | D. | ①④⑤⑥⑦ |
分析 ①纯铁不易构成原电池;
②钠与水反应生成可燃性气体氢气,过氧化钠与水反应生成助燃性气体氧气;
③铝在空气中耐腐蚀,与表面致密的氧化膜有关;
④钙主要存在于骨骼和牙齿中,缺钙易患佝偻病或发生骨质疏松,铁是血红蛋白的成分;
⑤青铜为Cu的合金、不锈钢为铁的合金、硬铝为铝的合金;
⑥KSCN溶液遇Fe3+离子,溶液为血红色;
⑦Al可发生铝热反应,Fe与水蒸气发生反应.
解答 解:①纯铁不易构成原电池,铁的合金易生锈,而纯铁不易生锈,故正确;
②钠与水反应生成可燃性气体氢气,过氧化钠与水反应生成助燃性气体氧气,则钠着火不能用水扑灭,应利用细沙扑灭,故错误;
③铝在空气中耐腐蚀,与表面致密的氧化膜有关,而Al为活泼金属,故错误;
④钙主要存在于骨骼和牙齿中,缺钙易患佝偻病或发生骨质疏松,铁是血红蛋白的成分,缺铁会引起贫血,故正确;
⑤青铜为Cu的合金、不锈钢为铁的合金、硬铝为铝的合金,均为常见的合金,故正确;
⑥KSCN溶液遇Fe3+离子,溶液为血红色,则KSCN溶液可以检验Fe3+离子,故正确;
⑦Al可发生铝热反应,Fe与水蒸气发生反应,则Al和Fe都能与某些氧化物反应,故正确;
故选D.
点评 本题考查金属及化合物的性质,为高频考点,把握物质的性质、发生的反应及相关反应原理等为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 规律 | 结论 |
| A | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS 沉淀中滴加CuSO4 溶液可以得到CuS 沉淀 |
| B | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| C | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| D | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3的沸点低于PH3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将溴水加入苯中 | 溴水颜色变浅 | 苯与溴水发生取代反应 |
| B | 将SO2通入到Ba(NO3)2溶液中 | 有白色沉淀 | 沉淀成分为BaSO3 |
| C | 等体积、等PH的HA和HB两种溶液分别与足量的锌反应 | 相同时间内,HA酸产生的氢气多 | HA为强酸 |
| D | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置 | 下层液体呈紫色 | Br2的氧化性强于I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化石燃料开采、加工过程常产生H2S废气,H2S的转化是资源利用和环境保护的重要课题.
化石燃料开采、加工过程常产生H2S废气,H2S的转化是资源利用和环境保护的重要课题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
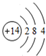 .
. ;V的氢氧化物作弱酸时有类似TR4-的离子产生,其电离方程式为Al(OH)3+H2O?H++[Al(OH)4]-.
;V的氢氧化物作弱酸时有类似TR4-的离子产生,其电离方程式为Al(OH)3+H2O?H++[Al(OH)4]-.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20gD2O所含电子数为10NA | |
| B. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 1molNa被氧化成Na2O2,失去电子数目为2NA | |
| D. | 氢气与氯气反应生成标准状况下22.4L氯化氢,断裂化学键总数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com