
【题目】下列说法正确的是( )
|
|
|
|
① | ② | ③ | ④ |
A.装置①表示已组装的铜锌原电池
B.装置②工作一段时间后,a极附近溶液的pH减小
C.装置③可以在铁钉上镀铜
D.装置④保护铁闸门不被腐蚀,为牺牲阳极的阴极保护法
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】1g氢气在氧气中燃烧生成液态水,放出142.9kJ的热量,表示该反应的热化学方程式是( )
A.H2(g)+1/2O2(g)![]() H2O(l)ΔH=-285.8kJ·mol-1
H2O(l)ΔH=-285.8kJ·mol-1
B.H2(g)+1/2O2(g)![]() H2O(g)ΔH=-285.8kJ·mol-1
H2O(g)ΔH=-285.8kJ·mol-1
C.2H2(g)+O2(g)![]() 2H2O(l)ΔH=-285.8kJ·mol-1
2H2O(l)ΔH=-285.8kJ·mol-1
D.H2+1/2O2![]() H2OΔH=-285.8kJ·mol-1
H2OΔH=-285.8kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O; c(NH4+) 由大到小的顺序是:①>②>③>④
B.某物质的溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,则该溶液的pH一定为14-a
C.物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+) +c(H+) =c(S2―) +c (HS―)+c (OH―)
D.AgCl悬浊液中存在平衡: AgCl(s)![]() Ag+(aq)+Cl―(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
Ag+(aq)+Cl―(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验不能达到预期实验目的是( )
序号 | 实验内容 | 实验目的 |
A | 将 | 配制质量分数为 |
B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
C | 将少量某有机物滴加到新制氢氧化铜悬浊液中,观察是否有红色沉淀生成 | 检验该有机物中是否含有醛基 |
D | 室温下,分别向2支试管中加入相同体积、相同浓度的 | 研究浓度对反应速率的影响 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应:Zn+2H+=H2↑+Zn2+,设计如图所示原电池,观察到Y电极上有气泡产生,下列说法错误的是( )
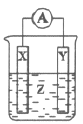
A.Y电极可能是铜
B.Z可能是硫酸铜溶液
C.电子流动方向:X→导线→Y
D.X电极的反应式:Zn-2e-=Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子能大量共存的是
A. pH=12的溶液中:K+、Na+、Br-、![]()
B. 无色溶液中:H+、K+、![]() 、
、![]()
C. c(Fe3+)=0.1mol·L-1的溶液中:K+、H+、SCN-、I-
D. 由水电离出的c(OH-)=1.0×10-13mol·L-1的溶液中:Na+、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一绝热容积不变的密闭容器中发生可逆反应![]() ,以下不能说明该反应达到化学平衡状态的是( )
,以下不能说明该反应达到化学平衡状态的是( )
A.混合气体的密度不再变化B.v逆(X)=v正(Y)
C.X、Y的浓度比为1:1D.体系压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,若开始时a、b两端液面相平,放置一段时间后,下列有关叙述中正确的是( )
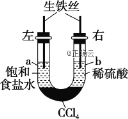
A.铁丝在两处的腐蚀速率:a>b
B.a、b两端相同的电极反应式为![]()
C.一段时间后,a端液面高于b端液面
D.a处总反应为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O
C.充电时,蓄电池的负极应与外接电源正极相连
D.放电时负极附近溶液的碱性减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com