
【题目】氮的化合物在工业生产和生活中都有重要的应用,运用化学原理研究氮的单质及其化合物具有重要意义。
I.一氯胺(NH2Cl)在中性或酸性环境中会发生水解,生成具有强烈杀菌作用的HClO,是重要的水的消毒剂。
(1)写出NH2C1的电子式______________________。
(2)写出NH2C1与水反应的化学方程式______________________。
(3)一定条件下(T℃、1.01×105Pa),可以用Cl2(g)和NH3(g)制得NH2Cl(g),同时得到HCl(g)。已知部分化学键的键能如下表:

写出该反应的热化学方程式____________________________________。
Ⅱ.亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在一定条件下合成:2NO(g)+Cl2(g) ![]() 2NOCl(g) △H<0。保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比
2NOCl(g) △H<0。保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比![]() 进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
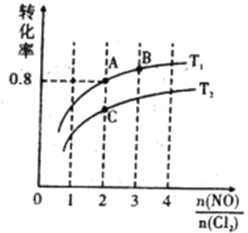
(4)图中T1、T2的关系为:T1______T2 (填“>”、“<”或“=”)
(5)图中纵坐标为物质__________的转化率,理由为___________________________。
(6)图中A、B、C三点对应的NOCl体积分数最大的是________(填“A”、“B”、或“C”)。
(7)若容器容积为1L,则B点的平衡常数为____________。
【答案】 ![]()
![]()
![]() < Cl2
< Cl2 ![]() 增加时Cl2的转化率增大(或其他合理表述均给分) A 80L/mol
增加时Cl2的转化率增大(或其他合理表述均给分) A 80L/mol
【解析】(1)NH2C1的电子式为![]() ;(2)NH2C1与水反应生成次氯酸和氨气,反应的化学方程式为
;(2)NH2C1与水反应生成次氯酸和氨气,反应的化学方程式为![]() ;(3)反应Cl2(g)+NH3(g)=NH2Cl(g)+HCl(g)的
;(3)反应Cl2(g)+NH3(g)=NH2Cl(g)+HCl(g)的![]() H=(+243.0+391.3
H=(+243.0+391.3![]() )kJ/mol= +11.3kJ/mol;(4)反应2NO(g)+Cl2(g)
)kJ/mol= +11.3kJ/mol;(4)反应2NO(g)+Cl2(g) ![]() 2NOCl(g) △H<0是放热反应,升高温度平衡逆向移动,转化率减小,故T1<T2;(5)随着氮氯比
2NOCl(g) △H<0是放热反应,升高温度平衡逆向移动,转化率减小,故T1<T2;(5)随着氮氯比![]() 增大,转化率增大,故图中纵坐标为物质Cl2的转化率,理由为
增大,转化率增大,故图中纵坐标为物质Cl2的转化率,理由为![]() 增加时Cl2的转化率增大;(6)升高温度平衡逆向移动,NOCl的体积分数减小,故A点NOCl体积分数比B点大;氮氯比
增加时Cl2的转化率增大;(6)升高温度平衡逆向移动,NOCl的体积分数减小,故A点NOCl体积分数比B点大;氮氯比![]() 越大,NO的转化率越小,NOCl的体积分数越小,故图中A、B、C三点对应的NOCl体积分数最大的是A点;(7)温度相同,化学平衡常数相同,则A点与B点平衡常数相同,A点氯气的转化率为0.8,
越大,NO的转化率越小,NOCl的体积分数越小,故图中A、B、C三点对应的NOCl体积分数最大的是A点;(7)温度相同,化学平衡常数相同,则A点与B点平衡常数相同,A点氯气的转化率为0.8,![]() =2,即NO和氯气的物质的量分别为2mol/L、1mol/L,则
=2,即NO和氯气的物质的量分别为2mol/L、1mol/L,则
2NO(g) + Cl2(g) ![]() 2NOCl(g)
2NOCl(g)
开始时浓度(mol/L) 2 1 0
改变的浓度(mol/L) 1.6 0.8 1.6
平衡时浓度(mol/L) 0.4 0.2 1.6
![]() =80 L/mol。
=80 L/mol。


科目:高中化学 来源: 题型:
【题目】下列有关糖类、油脂和蛋白质的说法正确的是
A. 油脂热量高,在生物体体内通过氧化提供能量
B. 从混合物中分离提纯蛋白质可采用过滤的方法
C. 淀粉、油脂和蛋白质都能在NaOH溶液中发生水解
D. 蔗糖及其水解产物都能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】垃圾的再生利用是垃圾资源化的最佳途径.某垃圾箱上贴有如右图所示标志,应向此垃圾箱中丢弃的垃圾是( ) 
A.废旧电池
B.厨余垃圾
C.危险废物
D.可回收物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
聚对萃二甲酸乙二醇酯(PET俗称涤纶树脂,是一种重要的有机高分子材料。其结构为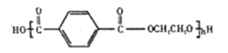 。利用有机物A合成PET的路线如下图所示:
。利用有机物A合成PET的路线如下图所示:
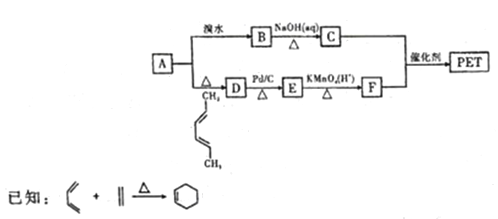
根据题意回答下列问题:
(1)B的化学名称是__________,C所含官能团的名称是____________________。
(2)由1,3-丁二烯可制备顺式聚1,3-丁二烯,写出顺式聚1,3-丁二烯的结构简式:________________________________________。
(3)A→D、B→C的反应类型分别为____________________、____________________。
(4)写出C+F→PET的化学反应方程式________________________________________。
(5)G是F的同系物,其相对分子质量比F多28,G的核磁共振氢谱有三组峰,峰面积比为3︰1︰1,则符合该条件的G的同分异构体共有__________种,写出其中一种结构简式____________________。
(6)参照上述合成路线,以1,3-丁二烯为原料(无机试剂任选),设计制备丁苯橡胶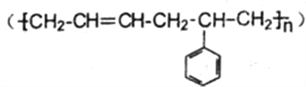
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组得到一块软锰矿样品,其主要成分为二氧化锰( MnO2)和石英(SiO2).为了制取Cl2和探究氯及其化合物的相关性质,进行如下实验.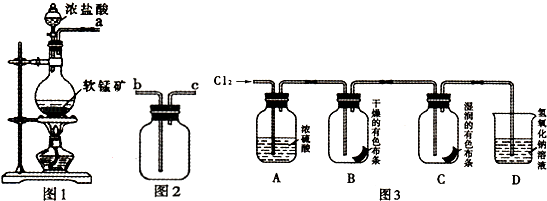
【查阅资料】MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)【制取气体】
取适量矿样置于烧瓶中,加入足量浓盐酸并加热,充分反应后烧瓶中残留的固体是 .
(2)收集氯气应将图1导管的a接口与图2导管的接口连接(填“b”或“c).
(3)若生成标准状况下11.2L Cl2 , 则参加反应的MnO2的物质的量为 mol.
(4)【实验探究】
把红热的铁丝伸入盛有氯气的集气瓶中,铁丝燃烧产生棕褐色的烟.反应的化学方程是 .
(5)按图3进行实验,观察到B中的有色布条不褪色,C中的有色布条褪色.由此得出的结论 .
(6)写出C中反应的化学方程式: .
(7)【联系实际】
某氯碱工厂的氯气管道发生泄漏,以下采取的措施正确的是 (填序号).
A.将人群向高处疏散
B.将人群向低处疏散
C.关闭氯气管道,用碱液浸泡过的棉布覆盖泄漏部位
D.关闭氯气管道,用饱和NaCl溶液浸泡过的棉布覆盖泄漏部位.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 等质量的CH4和苯完全燃烧耗氧量后者更大
B. SO2使溴水褪色与乙烯使酸性KMnO4褪色原理相同
C. 油脂皂化反应得到高级脂肪酸和甘油
D. 纤维素、聚乙烯、光导纤维都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,把0.2molL﹣1的醋酸加水稀释,则图中的纵轴y表示的是( ) 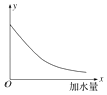
A.溶液中OH﹣的物质的量浓度
B.溶液的导电能力
C.溶液中的 ![]()
D.CH3COOH的电离程度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com