
分析 (1)防止食品被氧气氧化,则防腐剂应具有还原性;
(2)Fe3+转化为Fe2+为被还原的过程;
(3)反应3Cl2+2NH3=N2+6HCl中,Cl元素化合价降低,被还原,Cl2为氧化剂,N元素化合价升高,被氧化,NH3为还原剂,NH3可与HCl反应生成氯化铵,有白烟生成,以此解答.
解答 解:(1)防止食品被氧气氧化,则防腐剂应具有还原性,故答案为:还原性;
(2)Fe3+转化为Fe2+为被还原的过程,则维生素C起到还原剂的作用,具有还原性,故答案为:还原剂;
(3)A.反应生成HCl,NH3可与HCl反应生成氯化铵,有白烟生成,故A正确;
B.Cl元素化合价降低,被还原,Cl2为氧化剂,故B正确;
C.该反应属于置换反应,也属于氧化还原反应,故C错误;
D.N元素化合价由-3价升高到0价,则生成1molN2时有6mol电子转移,故D正确.
故选C.
点评 本题考查氯气的性质,侧重于化学与生活、生产的联系以及氧化还原反应的考查,注意从元素化合价的角度解答该题,难度不大.


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol | B. | 0.15 mol | C. | 0.22 mol | D. | 0.05 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓正确 | |
| B. | 向碳酸镁中加入稀盐酸:CO32-+2H+═CO2↑+H2O 错误,碳酸镁不应该写成离子形式 | |
| C. | 向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-═BaSO4↓正确 | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++2OH-+2H++SO42-═CaSO4↓+2H2O 错误,反应物和产物的配比不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(M+)>C(OH-)>C(A-)>C(H+) | B. | C(M+)>C(A-)>C(H+)>C(OH-) | ||
| C. | C(M+)>C(A-)>C(OH-)>C(H+) | D. | C(M+)+C(H+)>C(A-)+C(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
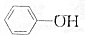 ,③
,③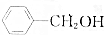 ,④CH3COOH,⑤CH3COOCH3,⑥CH2=CH-CH2OH.根据官能团的不同可分为( )
,④CH3COOH,⑤CH3COOCH3,⑥CH2=CH-CH2OH.根据官能团的不同可分为( )| A. | 3类 | B. | 4类 | C. | 5类 | D. | 6类 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com